题目内容
【题目】(1)5.3g Na2CO3的物质的量为____________,将其配成500mL溶液,所得溶液中Na2CO3的物质的量浓度为____________。取出该溶液10mL,在取出的溶液中通入HCl气体到不再产生气泡为止,共消耗____________mL HCl气体(标准状况)。
(2)V mL Al2(SO4)3溶液中,含有Al 3+m g,则溶液中SO42-的物质的量浓度为_______。(用含有m、V的式子表示)
【答案】0.05mol 0.1mol/L 44.8 ![]() mol/L
mol/L
【解析】
(1)5.3g碳酸钠的物质的量为:![]() =0.05mol,将0.05mol碳酸钠配成500mL溶液,所得溶液中Na2CO3的物质的量浓度为:
=0.05mol,将0.05mol碳酸钠配成500mL溶液,所得溶液中Na2CO3的物质的量浓度为:![]() =0.1mol/L,碳酸钠与氯化氢反应的关系式为:Na2CO3~2HCl,消耗的氯化氢的物质的量为:n(HCl)=2n(Na2CO3)=0.1mol/L×0.01L×2=0.002mol,标准状况下氯化氢的体积为:22.4L/mol×0.002mol=0.0448L=44.8mL;
=0.1mol/L,碳酸钠与氯化氢反应的关系式为:Na2CO3~2HCl,消耗的氯化氢的物质的量为:n(HCl)=2n(Na2CO3)=0.1mol/L×0.01L×2=0.002mol,标准状况下氯化氢的体积为:22.4L/mol×0.002mol=0.0448L=44.8mL;
(2)mg铝离子的物质的量为:![]() =
=![]() mol,根据化学式Al2(SO4)3,VmL硫酸铝溶液中含有的硫酸根离子的物质的量为:
mol,根据化学式Al2(SO4)3,VmL硫酸铝溶液中含有的硫酸根离子的物质的量为:![]() mol
mol![]() =
=![]() mol,溶液中SO42-的物质的量浓度为:
mol,溶液中SO42-的物质的量浓度为: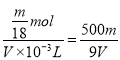 mol/L。
mol/L。

练习册系列答案
相关题目
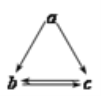
【题目】下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
a | b | c | |
A | Al2O3 | AlCl3 | Al(OH)3 |
B | NH3 | NO | NO2 |
C | Si | SiO2 | H2SiO3 |
D | Fe | FeCl2 | FeCl3 |
A.AB.BC.CD.D