题目内容
【题目】A、B、C、D、E五种物质是含钠元素的单质或化合物,其中B为淡黄色固体,它们有如图所示的转化关系:
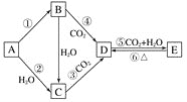
(1)推断各符号所代表的物质的化学式:A__,B__,C__,D__,E__。
(2)写出反应②的化学方程式:___。
(3)向D的饱和溶液中通入CO2时,反应的化学方程式为__。
【答案】Na Na2O2 NaOH Na2CO3 NaHCO3 2Na+2H2O=2NaOH+H2↑ CO2+H2O+Na2CO3=2NaHCO3↓
【解析】
A、B、C、D、E五种物质是含钠元素的单质或化合物,其中B为淡黄色的固体,能与二氧化碳、水反应,故B为Na2O2,D与二氧化碳和水反应生成E,E加热可生成D,则D为Na2CO3,E为NaHCO3,再转化关系可知,A为Na,C为NaOH。
(1)根据分析可知A为Na,B为Na2O2,C为NaOH,D为Na2CO3,E为NaHCO3;
(2)反应②为钠单质和水的反应,方程式为2Na+2H2O=2NaOH+H2↑;
(3)饱和碳酸钠溶液与二氧化碳反应生成碳酸氢钠,碳酸氢钠的溶解度小于碳酸钠,所以会与碳酸氢钠晶体析出,所以化学方程式为:CO2+H2O+Na2CO3=2NaHCO3↓。

【题目】如图为元素周期表的一部分,已知D为金属元素且其原子核外内层电子数为最外层电子数的5倍
A | B | C | ||||
D | E | X | ||||
G | ||||||
Y |
请回答下列问题:
(1)元素B在元素周期表中的位置为________
(2)元素A和元素E的最简单氢化物中沸点较高的是_____(填化学式)
(3)已知BC2中所有原子的最外层均满足8电子稳定结构,则BC2的电子式为_____其中B元素的化合价为______价。
(4)D3A2与H2O反应可生成两种碱,请写出该反应的化学方程式____________
(5)Y与X的原子序数之差为____________.