题目内容
下列有关物质性质的比较,正确的是
| A.热稳定性:HF<HCl<HBr | B.微粒半径: O2->Mg2+>Cl- |
| C.第一电离能:Si>Al>Mg | D.电负性:Si>Al>Mg |
D
试题分析:A、氟、氯、溴的非金属性逐渐减弱,所以气态氢化物的稳定性逐渐减弱,错误;B、Cl-比O2-、Mg2+多一个电子层,半径最大,错误;C、Mg的最外层电子是全充满状态,比较稳定,而Al的最外层的3p轨道上只有1个电子,较易失去,所以Mg的第一电离能大于Al,错误;D、Si、Al、Mg属于同周期元素,随核电荷数的增加,电负性逐渐增强,正确,答案选D。

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
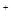 <Mg
<Mg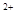 <Al
<Al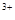 <O
<O
 >Na
>Na