题目内容
(1)32Ge原子核外电子有 种不同的运动状态,原子核外电子排布式为 。
(2)写出氮原子的核外电子的轨道表示式 。
(3)写出CCl4的电子式 ,其中心原子的杂化方式 。
(2)写出氮原子的核外电子的轨道表示式 。
(3)写出CCl4的电子式 ,其中心原子的杂化方式 。
(1)32 1s22s22p63s23p63d104s24p2;
(2)1s 2s
2s 2p
2p
(3)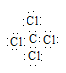 sp3杂化
sp3杂化
(2)1s
 2s
2s 2p
2p
(3)
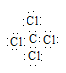 sp3杂化
sp3杂化试题分析:(1)电子的运动状态是由电子层数、电子亚层、原子轨道、自旋方向所决定的,所以任何一个原子里不存在运动状态相同的两个电子,所以核外有多少电子,就有多少种运动状态,32Ge原子核外电子有32种不同的运动状态,原子核外电子排布式为1s22s22p63s23p63d104s24p2;
(2)氮原子的核外电子的轨道表示式1s
 2s
2s 2p
2p
(3)根据电子式的书写原则,CCl4的电子式为
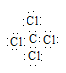 , CCl4的空间构型是正四面体,其中心原子的杂化方式sp3杂化。
, CCl4的空间构型是正四面体,其中心原子的杂化方式sp3杂化。
练习册系列答案
相关题目