��Ŀ����
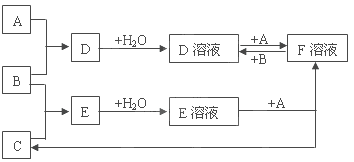
����Ŀ����֪A��B��CΪ��ѧ��ѧ�г����ĵ��ʣ���������AΪ���壬B��CΪ���壬��D��Һ�м���KSCN��Һ����Һ�Ժ�ɫ�������˵������¿ɷ������¹�ϵ�Ļ�ѧ��Ӧ��
�ش��������⣺
��1��A��B��C�ֱ���ʲô���ʣ�A______B________C________��
��2��д��D��Һ��ͨ��SO2�����ӷ���ʽ��____________________��
��3������amolFeI2��bmolFeBr2����Һ��ͨ��cmol����B����I-��Fe2+��Br-����ȫ����ʱcΪ��_____(��a��b��ʾ)��
���𰸡�����Fe�� ������Cl2�� ������H2�� 2Fe3++SO2+2H2O=SO42-+2Fe2++4H+ ![]() (a+b)
(a+b)
��������
A��B��CΪ��ѧ��ѧ�г����ĵ��ʣ���������AΪ���壬B��CΪ���壬A��B������Ӧ����D����D��Һ�м���KSCN��Һ����Һ�Ժ�ɫ��˵��D�к���Fe3+������A��Fe��B��Cl2��D��FeCl3��FeCl3�������ԣ�����������Ӧ������Ȼ���������FeCl3��Һ�м���Fe������Ӧ��2FeCl3 +Fe=3FeCl2��F��FeCl2��FeCl2���л�ԭ�ԣ���FeCl2��Һ��ͨ��������������Ӧ��2FeCl2+ Cl2=2FeCl3��B��C������Ӧ����E��E��Һ��Fe������Ӧ��������C��FeCl2����C��H2��E��HCl�������Ϸ������
A��B��CΪ��ѧ��ѧ�г����ĵ��ʣ���������AΪ���壬B��CΪ���壬A��B������Ӧ����D����D��Һ�м���KSCN��Һ����Һ�Ժ�ɫ��˵��D�к���Fe3+������A��Fe��B��Cl2��D��FeCl3��FeCl3�������ԣ�����������Ӧ������Ȼ���������FeCl3��Һ�м���Fe������Ӧ��2FeCl3 +Fe=3FeCl2��F��FeCl2��FeCl2���л�ԭ�ԣ���FeCl2��Һ��ͨ��������������Ӧ��2FeCl2+ Cl2=2FeCl3��B��C������Ӧ����E��E��Һ��Fe������Ӧ��������C��FeCl2����C��H2��E��HCl��
��1����������������֪A��Fe��B��Cl2��C��H2��
��2��FeCl3��ǿ�������ԣ���SO2���л�ԭ�ԣ���������Һ�ᷢ��������ԭ��Ӧ�������Ȼ����������ᣬ��Ӧ�����ӷ���ʽ�ǣ�2Fe3++SO2+2H2O==SO42-+2Fe2++4H+��
��3������amolFeI2��bmolFeBr2����Һ��ͨ��cmol����B��I-��Fe2+��Br-���л�ԭ�ԣ�������������������Ӧ����Ӧ����ʽ�ǣ�2FeI2+ 3Cl2=2FeCl3+ 2I2��2FeBr2+ 3Cl2=2FeCl3+ 2Br2��amolFeI2��Ӧ����![]() mol������bmolFeBr2��Ӧ����
mol������bmolFeBr2��Ӧ����![]() mol���������е�I-��Fe2+��Br-����ȫ����ʱcΪc=
mol���������е�I-��Fe2+��Br-����ȫ����ʱcΪc=![]() mol+
mol+![]() mol=
mol=![]() (a+b) mol��
(a+b) mol��

����Ŀ���ҹ��Ǹ������������������Ϊ�����һ����¯��������Ϊ�ձ������������
I.��֪��Ӧ![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]() Fe(s)+CO2(g)��H=-23.5kJmol-1���÷�Ӧ��1000����ƽ�ⳣ������4����һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol��Ӧ����l0min��ﵽƽ�⡣
Fe(s)+CO2(g)��H=-23.5kJmol-1���÷�Ӧ��1000����ƽ�ⳣ������4����һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol��Ӧ����l0min��ﵽƽ�⡣
(1)CO��ƽ��ת����=__��
(2)�����CO��ƽ��ת���ʣ��ٽ�Fe2O3��ת�����ɲ�ȡ�Ĵ�ʩ��__��
a.��߷�Ӧ�¶�
b.����Ӧ��ϵ��ѹǿ
c.ѡȡ���ʵĴ���
d.��ʱ���ջ��Ƴ�����CO2
e.�����ʯ��ʹ����ƽ���������ֽӴ�
��.��¯���������ķ����е�CO�ɽ��л��գ�ʹ����һ�������º�H2��Ӧ�Ʊ��״���CO(g)+2H2(g)![]() CH3OH(g)�������ͼʾ�ش��������⣺
CH3OH(g)�������ͼʾ�ش��������⣺
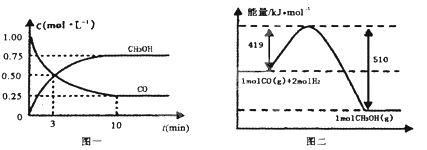
(3)�ӷ�Ӧ��ʼ��ƽ�⣬��H2Ũ�ȱ仯��ʾƽ����Ӧ����v(H2)=___��
(4)��֪������ȼ����286kJ/mol����д���״����岻���ȼ�յ��Ȼ�ѧ����ʽ___��
(5)�����¶Ⱥ�������ͬ�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ���÷�Ӧ�ﵽƽ�ⅼ���й��������±���
���� | ��Ӧ��Ͷ����� | ��Ӧ��� ת���� | CH3OH ��Ũ�� | �����仯(Q1��Q2��Q3������0) |
�� | 1molCO��2molH2 | ��1 | c1 | �ų�Q1kJ���� |
�� | 1molCH3OH | ��2 | c2 | ����Q2kJ���� |
�� | 2molCO��4molH2 | ��3 | c3 | �ų�Q3kJ���� |
�����й�ϵ��ȷ����___��
A.c1=c2 B.2Q1=Q3 C.2��1=��3 D.��/span>1+��2=1
E.�÷�Ӧ������1molCH3OH����ų�(Q1+Q2)kJ����
��.�Լ���Ϊȼ�ϵ����͵�أ���ɱ�����������Ϊȼ�ϵĴ�ͳȼ�ϵ�أ�Ŀǰ�õ��㷺���о�����ͼ��Ŀǰ�о��϶��һ�����������ȼ�ϵ�ع���ԭ��ʾ��ͼ���ش��������⣺
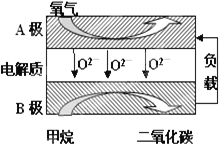
(6)B���ϵĵ缫��ӦʽΪ___��
(7)���ø�ȼ�ϵ������Դ����ʯī���缫���100mL1mol/L������ͭ��Һ���������ռ���������������ʱ�����������ĵļ�������Ϊ__(�����)��