题目内容
1.工业利用含有Al2O3、SiO2和少量FeO•xFe2O3的铝灰制备硫酸铝晶体与三草酸合铁酸钾[K2Fe(C2O4)3•3H2O]在的流程如图所示: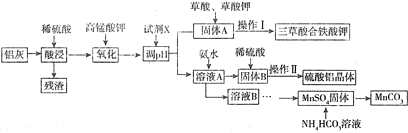
已知:生成氢氧化物的pH
| Al(OH)3 | Fe(OH)3 | |
| 开始沉淀时 | 3.6 | 2.1 |
| 完全沉淀时 | 5.2 | 3.2 |
(1)为提高酸浸速率,应采用的措施是(答出两条)适当提高硫酸的浓度、加热、搅拌,残渣的主要成分是SiO2;
(2)写出氧化过程中反应的了新方程式MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
(3)试剂X的化学式是Al2O3或Al(OH)3,pH的调控范围是3.2≤pH<3.6;
(4)操作Ⅱ的晶体步骤为蒸发浓缩、降温结晶,过滤洗涤、低温干燥,若操作Ⅰ与操作Ⅱ相同,则洗涤三草酸合铁酸钾以获得干燥晶体的试剂最好是b;
a.先热水后酒精 b.先冷水后酒精 c.先酒精后热水 d.先酒精后冷水
(5)生成MnCO3沉淀的离子方程式为Mn2++2HCO3-=MnCO3↓+H2O+CO2↑.
分析 铝灰(含Al、Al2O3及少量SiO2和FeO•xFe2O3),加入过量稀硫酸酸溶过滤,滤液为硫酸铝、硫酸亚铁、硫酸铁,残渣为二氧化硅和不溶性杂质,过滤后在滤液中加入稍过量高锰酸钾溶液氧化亚铁离子为铁离子,用氧化铝或氢氧化铝调节溶液PH使铁离子全部沉淀,铝离子不沉淀,得固体A为氢氧化铁,溶液A中含有铝离子,溶液A中加入氨水后得固体B为氢氧化铝,固体B中加入稀硫酸得硫酸铝溶液,再将硫酸铝溶液蒸发浓缩、降温结晶过滤洗涤得到硫酸铝钾晶体,溶液B中含有锰离子和硫酸根离子,硫酸锰固体溶于碳酸氢铵溶液可得碳酸锰沉淀,根据元素守恒可书写化学方程式,据此答题.
解答 解:铝灰(含Al、Al2O3及少量SiO2和FeO•xFe2O3),加入过量稀硫酸酸溶过滤,滤液为硫酸铝、硫酸亚铁、硫酸铁,残渣为二氧化硅和不溶性杂质,过滤后在滤液中加入稍过量高锰酸钾溶液氧化亚铁离子为铁离子,用氧化铝或氢氧化铝调节溶液PH使铁离子全部沉淀,铝离子不沉淀,得固体A为氢氧化铁,溶液A中含有铝离子,溶液A中加入氨水后得固体B为氢氧化铝,固体B中加入稀硫酸得硫酸铝溶液,再将硫酸铝溶液蒸发浓缩、降温结晶过滤洗涤得到硫酸铝钾晶体,溶液B中含有锰离子和硫酸根离子,硫酸锰固体溶于碳酸氢铵溶液可得碳酸锰沉淀,
(1)为提高酸浸速率,可以适当提高硫酸的浓度、加热、搅拌等,根据上面的分析可知,残渣的主要成分是SiO2,
故答案为:适当提高硫酸的浓度、加热、搅拌;SiO2;
(2)图中氧化过程就是高锰酸钾将亚铁离子氧化为铁离子,反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,
故答案为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
(3)根据上面的分析可知,试剂X的化学式是Al2O3或Al(OH)3,要使铁离子完全沉淀且铝离子不能沉淀,所以pH的调控范围是3.2≤pH<3.6,
故答案为:Al2O3或Al(OH)3;3.2≤pH<3.6;
(4)操作Ⅱ就是从硫酸铝溶液中得到硫酸铝晶体,步骤为 蒸发浓缩、降温结晶、过滤洗涤、低温干燥,若操作Ⅰ与操作Ⅱ相同,则洗涤三草酸合铁酸钾以获得干燥晶体的试剂最好是先冷水后酒精,这样即可以除去可溶性杂质,又可以减小三草酸合铁酸钾的溶解,又便于干燥,故选b,
故答案为:蒸发浓缩、降温结晶;b;
(5)生成MnCO3沉淀的离子方程式为Mn2++2HCO3-=MnCO3↓+H2O+CO2↑,故答案为:Mn2++2HCO3-=MnCO3↓+H2O+CO2↑.
点评 本题考查了流程分析,反应过程理解应用,反应现象和产物的判断,注意基本实验的操作步骤,离子方程式书写等,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 加入浓硫酸 | B. | 煮熟 | C. | 变性 | D. | 盐析 |
| A. | 双氧水可用于皮肤伤口消毒 | |
| B. | 水玻璃是制备硅胶和木材防火剂等的原料 | |
| C. | 生石灰和铁粉都是食品包装中常用的干燥剂 | |
| D. | 生活中可用电解饱和食盐水的方法制取消毒液 |
粗铜$\stackrel{Cl_{2}}{→}$固体$\stackrel{加稀盐酸溶液}{→}$溶液Ⅰ$\stackrel{调节溶液pH}{→}$

已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| 金属离子 | Fe3+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 6.7 |
(1)溶液Ⅰ之所以要调节溶液pH,目的是除去Fe3+且不引人杂质.调节溶液pH时,理论上可选择pH最大范围是3.2≤pH<4.7.
(2)由溶液Ⅱ制备CuCl2•2H2O的操作依次为:边滴加浓盐酸边加热浓缩、冷却结晶、过滤(填操作名称)、洗涤干燥.
(3)某学习小组用碘量法测定CuCl2•2H2O样品的纯度(杂质不参与反应),实验如下:
a.准确称取CuCl2•2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250mL待测溶液.(已知:2Cu2++4I-═2Cu↓+I2)
b.移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用cmol•L-1Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为VmL.(已知:I2+2S2O32-═2I-+S4O62-)则该样品中CuCl2•2H2O的质量分数为$\frac{1.71cV}{m}$×100%(用含m,c,V的代数式表示,不用化简).如果达到滴定终点时,仰视滴定管读数将使测定结果偏高(填“偏高”、“偏低”或“无影响”).
(4)已知热化学方程式:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ•mol-1;
2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJ•mol-1.则由辉铜矿(Cu2S)制取铜的热化学方程式为3Cu2S(s)+3O2(g)=6Cu(s)+3SO2(g),故△H=-652.2kJ•mol-1.

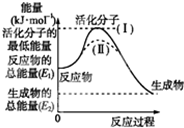 请认真观察图,然后回答问题:
请认真观察图,然后回答问题: