题目内容
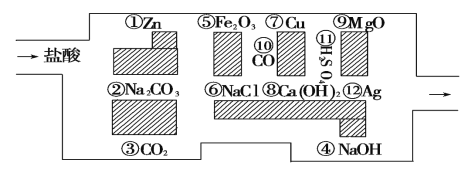
【题目】如图表示的是A→E五种物质的相互转化关系,其中A为淡黄色固体,B为单质,D为正盐。

请回答下列问题:
(1)写出各物质的名称:
A_____________ ; C_____________;D_____________。
(2)写出相应的离子方程式:
B→C: _____________________________;
C→D: ______________________________;
A→C: _____________________________;
D→E:_____________________________(任写一个即可)。
【答案】过氧化钠 氢氧化钠 碳酸钠 2Na+2H2O==2Na++2OH-+H2↑ 2OH-+CO2==CO32—+H2O 2Na2O2+2H2O==4Na++4OH-+ O2↑ CO32—+2H+==CO2↑+H2O
【解析】
(1)淡黄色固体A能与二氧化碳、水反应,则A为Na2O2,A与水反应生成C,与二氧化碳反应生成D,且C与二氧化碳反应生成D,则C为NaOH、D为碳酸钠,B与水反应生成C,与氯气反应生成E,则B为Na,E为NaCl,故答案为:过氧化钠;氢氧化钠;碳酸钠;
(2)B→C的反应为钠与水反应生成氢氧化钠和氢气,反应的离子方程式为:2Na+2H2O==2Na++2OH-+H2↑,故答案为:2Na+2H2O==2Na++2OH-+H2↑;
C→D的反应为氢氧化钠溶液与二氧化碳反应生成碳酸钠和水,反应的离子方程式为:2OH-+CO2==CO32—+H2O,故答案为:2OH-+CO2==CO32—+H2O;
A→C的反应为过氧化钠与水反应生成氢氧化钠和氧气,反应的离子方程式为:2Na2O2+2H2O==
4Na++4OH-+ O2↑,故答案为:2Na2O2+2H2O==4Na++4OH-+ O2↑;
D→E的反应为碳酸钠与盐酸反应生成碳酸氢钠和氯化钠或二氧化碳、氯化钠和水,反应的离子方程式为:CO32—+H+==HCO3—或CO32—+2H+==CO2↑+H2O,故答案为:CO32—+H+==HCO3—或CO32—+2H+==CO2↑+H2O。

 阅读快车系列答案
阅读快车系列答案【题目】海水是一个巨大的化学资源宝库,利用海水可以获得很多化工产品。
(1)海水中制得的氯化钠可用于生产烧碱及氯气。反应的离子方程式是 。
(2)利用制盐后的盐卤提取溴的工艺流程如下(部分操作和条件已略去):
![]()
将Br2与Na2CO3反应的化学方程式补充完整:
![]()
(3)盐卤蒸发冷却后析出卤块的主要成分是MgCl2,此外还含Fe2+、Fe3+、Mn2+等离子。以卤块为原料制得镁的工艺流程如下(部分操作和条件已略去):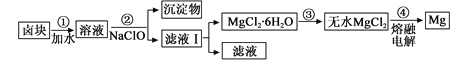
生成氢氧化物沉淀的pH
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH) 2 | 9.6 | 11.1 |
①步骤②中需控制pH=9.8,其目的是 。
②用NaClO 氧化Fe2+得到Fe(OH)3沉淀的离子反应方程式是 。
③步骤③需在HCl保护气中加热进行,请用化学平衡移动原理解释原因________。
④NaClO还能除去盐卤中的CO(NH2)2,生成盐和能参与大气循环的物质。除去0.1mol CO(NH2)2时消耗
NaClO g。