题目内容
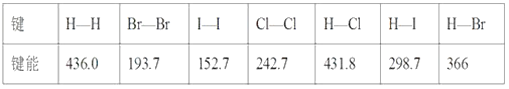
【题目】25℃时,Ksp[Mg(OH)2]=10-12,Ksp(MgF2)=10-10。下列说法正确的是( )
A. 25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)减小
B. 25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大
C. 25℃时,Mg(OH)2固体在20mL 0.01 molL-1氨水中的Ksp比在20mL 0.01 molL-1NH4Cl溶液中的Ksp小
D. 25℃时,欲用1L NaF溶液将0.05mol Mg(OH)2完全转化为MgF2,则c(NaF)≥1.1 molL-1
【答案】D
【解析】25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,![]() 结合Mg(OH)2电离的OH-,使Mg(OH)2的沉淀溶解平衡正向移动,c(Mg2+)增大,故A错误;Ksp[Mg(OH)2]<Ksp(MgF2),所以饱和Mg(OH)2溶液与饱和MgF2溶液相比,后者的c(Mg2+)大,故B错误;25℃时,Mg(OH)2固体在20mL 0.01 molL-1氨水中的Ksp与在20mL 0.01 molL-1NH4Cl溶液中的Ksp相等,故C错误;用1L NaF溶液将0.05mol Mg(OH)2完全转化为MgF2,则转化后溶液中c(OH-)=0.1 molL-1, c(Mg2+)=
结合Mg(OH)2电离的OH-,使Mg(OH)2的沉淀溶解平衡正向移动,c(Mg2+)增大,故A错误;Ksp[Mg(OH)2]<Ksp(MgF2),所以饱和Mg(OH)2溶液与饱和MgF2溶液相比,后者的c(Mg2+)大,故B错误;25℃时,Mg(OH)2固体在20mL 0.01 molL-1氨水中的Ksp与在20mL 0.01 molL-1NH4Cl溶液中的Ksp相等,故C错误;用1L NaF溶液将0.05mol Mg(OH)2完全转化为MgF2,则转化后溶液中c(OH-)=0.1 molL-1, c(Mg2+)= ![]() 10-10 molL-1,c(F-)≥1 molL-1,生成MgF2消耗n(F-)=0.1 mol,所以原溶液c(NaF)≥1.1 molL-1,故D正确。
10-10 molL-1,c(F-)≥1 molL-1,生成MgF2消耗n(F-)=0.1 mol,所以原溶液c(NaF)≥1.1 molL-1,故D正确。

【题目】将牛奶和姜汁混合,待牛奶凝固便成为一种富有广东特色的甜品——姜撞奶。为了掌握牛奶凝固所需的条件,某同学在不同温度的等量牛奶中混人一些新鲜姜汁,观察混合物15min,看其是否会凝固,结果如下表。请回答下列问题:
温度(℃) | 20 | 40 | 60 | 80 | 100 |
结果 | 15min后仍未有凝固迹象 | 14min内完全凝固 | 1min内完全凝固 | 1min内完全凝固 | 15min后仍未有凝固迹象 |
(注:用曾煮沸的姜汁重复这项实验,牛奶在任何温度下均不能凝固)
(1)实验证明新鲜姜汁中含有一种酶,其作用是 。
(2)20℃和100℃时,15min后仍未有凝固迹象,说明酶的活性较低,其原因分别是 和 。
(3)若60℃时牛奶在有姜汁和没有姜汁的情况下都可以凝固,当反应进行到t时,向其中加人姜汁。下图中能正确表示加姜汁后牛奶凝固随时间变化趋势的曲线是 。
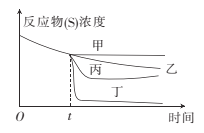
(4)为提高实验的准确度,实验中“不同温度的等量牛奶中混入一些新鲜姜汁”操作中应注意的是 。
(5)有同学说,该实验不能得出姜汁使牛奶凝固的最适温度,请提出解决方案: 。