题目内容
【题目】下列说法中正确的是
A. 6.8g固体KHSO4与3.9g固体Na2O2中阴离子数目相同
B. 常温下铁、铜均不溶于浓硫酸,说明常温下铁、铜与浓硫酸均不反应
C. 离子化合物中只含离子键
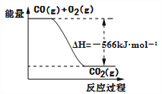
D. 已知:2CO(g)+O2(g)=2CO2(g);ΔH=-566kJ·mol-1,下图可表示由CO生成CO2的反应过程和能量关系
【答案】A
【解析】A、NaHSO4固体中阴离子是HSO4-,6.8gNaHSO4固体含有阴离子物质的量为6.8×1/136mol=0.05mol,Na2O2中阴离子是O22-,3.9gNa2O2中阴离子物质的量为3.9×1/78mol=0.05mol,故A正确;B、常温下,铁与浓硫酸发生钝化反应,故B错误;C、有的离子化合物中除含有离子键外,还含有共价键,如NaOH,既含有离子键又含有共价键,故C错误;D、此反应是放热反应,2CO2和O2总能量比CO2的总能量高,应是2CO2和O2的反应生成CO2,故D错误。

练习册系列答案
相关题目