جâؤ؟ؤعبف
،¾جâؤ؟،؟£¨1£©سذ¼×،¢ززء½ضضخïضت£؛¼×![]() ،¢زز
،¢زز![]() ،£سة¼××ھ»¯خھززذè¾دآءذ¹³ج
،£سة¼××ھ»¯خھززذè¾دآءذ¹³ج![]() زرآشب¥¸÷²½·´س¦µؤخق¹ط²ْخدآح¬
زرآشب¥¸÷²½·´س¦µؤخق¹ط²ْخدآح¬![]()
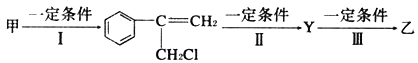
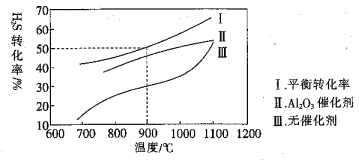
¢ظ·´س¦Iµؤ·´س¦ہàذحتا__________£¬·´س¦IIµؤجُ¼تا___________£¬·´س¦IIIµؤ»¯ر§·½³جت½خھ_________________________
¢عدآءذخïضت²»ؤـسëزز·´س¦µؤتا_________![]() جîذٍ؛إ
جîذٍ؛إ![]() ،£
،£
![]() ½ًتôؤئ
½ًتôؤئ ![]() نهث®
نهث® ![]() اâرُ»¯ؤئبـز؛
اâرُ»¯ؤئبـز؛ ![]() ززثل
ززثل
£¨2£©ذ´³ِ±½·س؛حج¼ثلؤئبـز؛·´س¦µؤہë×س·½³جت½__________________،£
£¨3£©ذ´³ِززب©؛حزّ°±بـز؛·´س¦µؤ»¯ر§·½³جت½____________________،£
£¨4£©ذ´³ِزز¶ثل؛حؤئ·´س¦µؤ»¯ر§·½³جت½______________________،£
،¾´ً°¸،؟ب،´ْ·´س¦ اâرُ»¯ؤئث®بـز؛،¢¼سبب ![]() +HCl،ْ
+HCl،ْ![]() b
b ![]() +CO32-،ْ
+CO32-،ْ![]() +HCO3- CH3CHO+2Ag(NH3)2OH
+HCO3- CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag،+3NH3+H2O HOOCCOOH+2Na،ْNaOOCCOONa+H2،ü
CH3COONH4+2Ag،+3NH3+H2O HOOCCOOH+2Na،ْNaOOCCOONa+H2،ü
،¾½âخِ،؟
(1)¢ظ¸ù¾فء÷³جح¼؟ةضھ£¬·´س¦Iخھ¹âصصجُ¼دآ£¬·¢ةْحé»ùاâش×سµؤب،´ْ·´س¦£¬·´س¦IIخھآ±´ْجشعNaOHث®بـز؛جُ¼دآµؤث®½âةْ³ة´¼£¬·´س¦IIIخھج¼ج¼ث«¼üسëHClµؤ¼س³ة·´س¦£¬¾ف´ث·ضخِ½â´ً£»
¢ع¸ù¾فززضذ؛¬سذ´¼ôا»ù؛حآ±ثطش×س£¬½ل؛د´¼؛حآ±´ْجµؤذشضت·ضخِ½â´ً£»
(2)±½·سؤـ¸ْج¼ثلؤئبـز؛·´س¦£¬ةْ³ة±½·سؤئ؛حج¼ثلاâؤئ£»
(3)ززب©سëزّ°±بـز؛·¢ةْزّ¾µ·´س¦ةْ³ة´×ثلï§،¢Ag،¢°±ئّ،¢ث®£»
(4)زز¶ثل؛حؤئ·´س¦ةْ³ةNaOOCCOONa؛حاâئّ،£
(1)¢ظسة¼××ھ»¯خھزز¹³ج؟ةضھ£¬·´س¦Iخھ¹âصصجُ¼دآ£¬·¢ةْحé»ùاâش×سµؤب،´ْ·´س¦£¬·´س¦IIخھNaOHث®بـز؛،¢¼سببجُ¼دآµؤث®½âةْ³ة´¼£¬·´س¦IIIخھج¼ج¼ث«¼üسëHClµؤ¼س³ة·´س¦£¬ئنضذ·´س¦IIIµؤ»¯ر§·½³جت½خھ£؛![]() +HCl،ْ
+HCl،ْ![]() £¬¹ت´ً°¸خھ£؛ب،´ْ·´س¦£»اâرُ»¯ؤئث®بـز؛،¢¼سبب£»
£¬¹ت´ً°¸خھ£؛ب،´ْ·´س¦£»اâرُ»¯ؤئث®بـز؛،¢¼سبب£»![]() +HCl،ْ
+HCl،ْ![]() £»
£»
¢عزز(![]() )ضذ؛¬سذ´¼ôا»ù£¬ؤـسëؤئ·´س¦£¬ؤـسëززثل·¢ةُْ¥»¯·´س¦£¬؛¬سذآبش×س£¬شعاâرُ»¯ؤئث®بـز؛،¢¼سببجُ¼دآ؟ةزش·¢ةْث®½â·´س¦£¬زز²»ؤـسëنهث®·´س¦£¬¹ت´ً°¸خھ£؛b£»
)ضذ؛¬سذ´¼ôا»ù£¬ؤـسëؤئ·´س¦£¬ؤـسëززثل·¢ةُْ¥»¯·´س¦£¬؛¬سذآبش×س£¬شعاâرُ»¯ؤئث®بـز؛،¢¼سببجُ¼دآ؟ةزش·¢ةْث®½â·´س¦£¬زز²»ؤـسëنهث®·´س¦£¬¹ت´ً°¸خھ£؛b£»
(2)±½·سؤـ¸ْج¼ثلؤئبـز؛·´س¦£¬ةْ³ة±½·سؤئ؛حج¼ثلاâؤئ£¬·´س¦µؤہë×س·½³جت½خھ![]() +CO32-،ْ
+CO32-،ْ![]() +HCO3-£¬¹ت´ً°¸خھ£؛
+HCO3-£¬¹ت´ً°¸خھ£؛![]() +CO32-،ْ
+CO32-،ْ![]() +HCO3-£»
+HCO3-£»
(3)ززب©سëزّ°±بـز؛·¢ةْزّ¾µ·´س¦ةْ³ةززثلï§،¢Ag،¢°±ئّ،¢ث®£¬·´س¦µؤ»¯ر§·½³جت½خھCH3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag،+3NH3+H2O£¬¹ت´ً°¸خھ£؛CH3CHO+2Ag(NH3)2OH
CH3COONH4+2Ag،+3NH3+H2O£¬¹ت´ً°¸خھ£؛CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+2Ag،+3NH3+H2O£»
CH3COONH4+2Ag،+3NH3+H2O£»
(4)زز¶ثل؛حؤئ·´س¦µؤ»¯ر§·½³جت½خھHOOCCOOH+2Na،ْNaOOCCOONa+H2،ü£¬¹ت´ً°¸خھ£؛HOOCCOOH+2Na،ْNaOOCCOONa+H2،ü،£

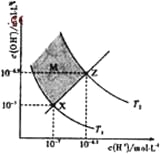
،¾جâؤ؟،؟²â¶¨0.1 mol،¤L-1 Na2SO3بـز؛دبةخآشظ½µخآ¹³جضذµؤpH£¬ت¾فبçدآ،£
ت±؟ج | ¢ظ | ¢ع | ¢غ | ¢ـ |
خآ¶ب/،و | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
تµرé¹³جضذ£¬ب،¢ظ¢ـت±؟جµؤبـز؛£¬¼سبëرخثلثل»¯µؤBaCl2بـز؛×ِ¶ش±بتµر飬¢ـ²ْةْ°×ة«³ءµي¶à،£
دآءذثµ·¨²»صب·µؤتا
A. Na2SO3بـز؛ضذ´وشعث®½âئ½؛â£؛![]() +H2O
+H2O![]()
![]() +OH
+OH
B. ¢ـµؤpHسë¢ظ²»ح¬£¬تاسةسع![]() إ¨¶ب¼ُذ،شى³ةµؤ
إ¨¶ب¼ُذ،شى³ةµؤ
C. ¢ظ،ْ¢غµؤ¹³جضذ£¬خآ¶ب؛حإ¨¶ب¶شث®½âئ½؛âزئ¶¯·½دٍµؤس°دىز»ضآ
D. ¢ظسë¢ـµؤKwضµدàµب
،¾جâؤ؟،؟A،«Gتا¶جضـئعض÷×هشھثط£¬ش×سذٍتزہ´خشِ´َ£¬²؟·ضشھثطµؤ²؟·ضذإد¢بçدآ±يثùت¾£؛
A | B | C | D | E | F | |
ش×س°ë¾¶/nm | 0.077 | 0.075 | 0.074 | 0.099 | ||
ض÷زھ »¯؛د¼غ | +4 -4 | +5 -3 | -2 | +6 -2 | ||
ئنثû | ز»ضضح¬خ»ثطش×سخقضذ×س | ثùسذسذ»ْخïضذز»¶¨؛¬سذµؤشھثط | ¼ٍµ¥ا⻯خï³£سأ×÷ضئہن¼ء | ¶جضـئعض÷×هشھثطضذش×س°ë¾¶×î´َ |
»ط´ًدآءذختج⣨سأدàس¦»¯ر§سأس£؛
£¨1£©Gشعضـئع±يضذµؤخ»ضأتا___£¬Fµؤ¼ٍµ¥ہë×س½ل¹¹ت¾زâح¼تا___،£
£¨2£©سةA،¢C،¢Gبضضشھثطذخ³ةµؤش×س¸ِت±بخھ4£؛1£؛1µؤ»¯؛دخïµؤµç×ست½خھ___£¬¸أ»¯؛دخïثù؛¬µؤ»¯ر§¼üسذ___،££¨جر§¼üہàذح£©
£¨3£©D،¢E،¢F،¢G¼ٍµ¥ہë×س°ë¾¶سةذ،µ½´َث³ذٍ___،£
£¨4£©سأµç×ست½±يت¾BD2µؤذخ³ة¹³ج___،£
£¨5£©C،¢D،¢Fµؤ¼ٍµ¥ا⻯خïضذ·ذµمسة¸كµ½µحµؤث³ذٍتا___،£
£¨6£©ذ´³ِE2D2؛حA2D·´س¦µؤ»¯ر§·½³جت½___£¬¸أ·´س¦أ؟دû؛ؤ1molE2D2µç×س×ھزئتؤ؟خھ___،£