题目内容
【题目】某同学进行如下实验,探究化学反应中的能量变化。
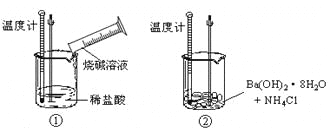
通过实验测出,反应前后①烧杯中的温度升高,②烧杯中的温度降低。由此判断NaOH溶液跟盐酸的反应是__________(填 “吸热”或“放热”)反应,Ba(OH)2· 8H2O跟NH4Cl的反应是____________(填“吸热”或“放热”)反应。反应①中反应物的总能量_____________填(“大于”、“小于”或“等于”)生成物的总能量。反应②中断开反应物中的化学键所吸收的能量_____________填(“大于”、“小于”或“等于”)形成生成物中的化学键所放出的能量。
【答案】放热 吸热 大于 大于
【解析】
探究化学反应中的能量变化时,温度升高,则反应放热,温度降低、反应吸热:放热反应中,反应物总能量大于生成物总能量;吸热反应中,反应物化学键断裂吸收能量大于生成物中化学键形成放热热量。
通过实验测出,反应前后①烧杯中的温度升高,②烧杯中的温度降低,根据温度升高,反应放热,温度降低、反应吸热,所以NaOH溶液跟盐酸的反应是放热反应,Ba(OH)2· 8H2O跟NH4Cl的反应是吸热反应;反应①为放热反应,则反应物的总能量大于生成物的总能量;反应②为吸热反应,则断开反应物中的化学键所吸收的能量大于形成生成物中的化学键所放出的能量;
因此,本题正确答案是:放热;吸热;大于;大于。

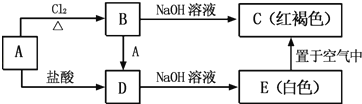
【题目】某研究小组同学欲探究某袋敞口放置一段时间的名为“硫酸亚铁家庭园艺精品肥料”的化肥的主要成分及相关性质。首先对该化肥的成分进行了如下假设:
a.只含有FeSO4
b.含有FeSO4和Fe2(SO4)3
c.只含有Fe2(SO4)3
将化肥固体粉末溶于水中得到溶液(记为X),进行如下实验:
实验序号 | 操作 | 现象 |
ⅰ | 取2 mL溶液X,加入1 mL 1 mol·L-1 NaOH溶液 | 产生红褐色沉淀 |
ⅱ | 取2 mL溶液X,加入1滴KSCN | 溶液显红色 |
(1)请用文字表述做出假设b的依据是__________________________。
(2)对实验ⅰ的预期现象是产生白色沉淀、变为灰绿色、最后出现红褐色沉淀,预期产生该现象的依据是(用化学方程式或离子方程式表达)_____、_____。
(3)由实验ⅱ得出的结论是____________。结合实验ⅰ、ⅱ,推测实验ⅰ实际现象与预期现象不符的原因可能是_____________________________。为进一步验证假设,小组同学进行了以下实验:
实验序号 | 操作 | 现象 |
ⅲ | 取2 mL溶液X,加入1滴KSCN,再加入1 mL水 | 溶液显红色 |
ⅳ | 取2 mL溶液X,加入1滴KSCN,再加入1 mL氯水 | 溶液显红色,颜色比ⅲ深 |
(4)实验ⅳ中氯水参加反应的离子方程式是_______________________。
(5)通过以上实验,可得到的结论是_____________________________,请完整表达该结论是如何得出的_______________________________。