题目内容
16.下列有关叙述中正确的是( )| A. | 滴定管下端连有橡皮管的为酸式滴定管 | |
| B. | 在滴定时,左手操作锥形瓶,右手操作滴定管开关 | |
| C. | 滴定前应首先排除尖嘴部分的气泡 | |
| D. | 滴定过程中两眼应注视滴定管内液面的变化 |
分析 A.滴定管下端连有橡皮管的为碱式滴定管;
B.滴定时左手控制酸式滴定管的玻璃活塞;
C.滴定前应排除尖嘴部分的气泡,否则影响待测液的体积;
D.滴定过程中两眼应注视锥形瓶中溶液颜色的变化.
解答 解:A.滴定管下端连有橡皮管的为碱式滴定管,酸式滴定管下端有活塞,故A错误;
B.在滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,故B错误;
C.滴定前应排除尖嘴部分的气泡,否则影响待测液的体积,形成误差,故C正确;
D.滴定过程中两眼应注视锥形瓶中溶液颜色的变化,以判断终点的到达,故D错误.
故选C.
点评 本题主要考查了滴定操作以及注意事项,注重了基础知识作的考查,本题难度不大.

练习册系列答案
相关题目
6.过氧化钙是一种重要的化工原料,温度在350℃以上容易分解.
(1)利用反应Ca(s)+O2$\frac{\underline{\;\;△\;\;}}{\;}$CaO2(s),在纯氧条件下,制取CaO2的装置示意图1如下:
请回答下列问题:
①装置A中反应的化学方程式为2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑;仪器a的名称为蒸馏烧瓶;
装置D中盛有的液体是浓硫酸,其作用一是观察氧气的流速,判断氧气通入是否过快及氧气与钙反应进行的程度;二是防止空气进入C装置影响产品纯度.仪器安装后应进行的实验操作:
a.通入氧气 b.检查装置气密性 c.加入药品 d.停止通氧气
e.点燃酒精灯 f.熄灭酒精灯 g.冷却至室温,
正确的操作顺序为bcaefgd.
②完全反应后,有关数据记录如下:
据此可判断m2与理论值不符,则产物中的杂质可能是CaO、Ca3N2等.
(2)利用反应Ca2++H2O2+2NH3•H2O+6H2O=CaO2•8H2O+2NH4+,在碱性环境中,制取CaO2的流程示意图2如下:
请回答下列问题:
①主反应中,NH3•H2O在Ca2+和H2O2的反应历程中所起的作用是中和过氧化氢和Ca2+反应析出的氢离子,促进反应进行;该反应所需的条件及操作为acf(填字母).
a.把氯化钙溶液逐滴加入过氧化氢-氨水溶液中
b.把过氧化氢-氨水溶液逐滴加入氯化钙溶液中
c.滴加时先搅拌后静置,观察晶体析出
d.滴加时不停搅拌,直至晶体完全析出
e.反应体系热水浴加热
f.反应体系冰水浴冷却
洗涤CaO2•8H2O晶体时,判断晶体是否完全洗净的试剂为AgNO3溶液;滤液循环使用时需在反应器中加入一种物质,该物质的化学式为Ca(OH)2.
②利用反应2CaO2 >350℃?2CaO+O2↑测量产品中CaO2含量时,停止反应且冷却至25℃后的装置示意图3如下:若直接读数确定25℃、1大气压下气体的体积,则测量结果偏大(填“偏大”、“偏小”或“无影响”).

(1)利用反应Ca(s)+O2$\frac{\underline{\;\;△\;\;}}{\;}$CaO2(s),在纯氧条件下,制取CaO2的装置示意图1如下:
请回答下列问题:
①装置A中反应的化学方程式为2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑;仪器a的名称为蒸馏烧瓶;
装置D中盛有的液体是浓硫酸,其作用一是观察氧气的流速,判断氧气通入是否过快及氧气与钙反应进行的程度;二是防止空气进入C装置影响产品纯度.仪器安装后应进行的实验操作:
a.通入氧气 b.检查装置气密性 c.加入药品 d.停止通氧气
e.点燃酒精灯 f.熄灭酒精灯 g.冷却至室温,
正确的操作顺序为bcaefgd.
②完全反应后,有关数据记录如下:
| 空瓷舟质量m0/g | 瓷舟与钙的质量m1/g | 瓷舟与产物的质量m2/g |
| 14.80 | 15.08 | 15.25 |
(2)利用反应Ca2++H2O2+2NH3•H2O+6H2O=CaO2•8H2O+2NH4+,在碱性环境中,制取CaO2的流程示意图2如下:
请回答下列问题:
①主反应中,NH3•H2O在Ca2+和H2O2的反应历程中所起的作用是中和过氧化氢和Ca2+反应析出的氢离子,促进反应进行;该反应所需的条件及操作为acf(填字母).
a.把氯化钙溶液逐滴加入过氧化氢-氨水溶液中
b.把过氧化氢-氨水溶液逐滴加入氯化钙溶液中
c.滴加时先搅拌后静置,观察晶体析出
d.滴加时不停搅拌,直至晶体完全析出
e.反应体系热水浴加热
f.反应体系冰水浴冷却
洗涤CaO2•8H2O晶体时,判断晶体是否完全洗净的试剂为AgNO3溶液;滤液循环使用时需在反应器中加入一种物质,该物质的化学式为Ca(OH)2.
②利用反应2CaO2 >350℃?2CaO+O2↑测量产品中CaO2含量时,停止反应且冷却至25℃后的装置示意图3如下:若直接读数确定25℃、1大气压下气体的体积,则测量结果偏大(填“偏大”、“偏小”或“无影响”).

7.在恒温、恒容的密闭容器中反应.若反应物的浓度由2mol/L降到0.8mol/L需20s,那么反应物浓度由2mol/L降到1.4mol/L所需的时间( )
| A. | 10s | B. | 大于10s | C. | 小于10s | D. | 无法判断 |
4.如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近呈蓝色.下列说法正确的是( )
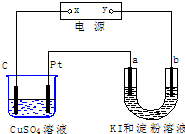

| A. | C是阳极,Pt是阴极 | |
| B. | x是负极,y是正极 | |
| C. | a极和Pt产生气体的物质的量相同 | |
| D. | CuSO4溶液pH值不变,U形管溶液pH值增大 |
11.下列说法正确的是( )
| A. | 强酸跟强碱反应放出的热量一定是中和热 | |
| B. | 1 mol酸与1 mol碱完全反应放出的热量是中和热 | |
| C. | 在稀溶液中,强酸与强碱发生中和反应生成1 mol H2O(l)时的反应热叫做中和热 | |
| D. | 表示中和热的离子方程式为H++OH-═H2O△H=-57.3 kJ/mol |
8.影响化学反应速率的主要因素是( )
| A. | 温度 | B. | 压强 | C. | 反应物本身性质 | D. | 催化剂 |
5.氢化钙可以作为生氢剂(其中CaH2中氢元素为-1价),反应方程式如下:CaH2+2H2O═Ca(OH)2+2H2↑,下列叙述正确的是( )
| A. | H2O既不是氧化剂也不是还原剂 | B. | Ca(OH)2是氧化产物 | ||
| C. | 生成1molH2转移的电子数为2NA | D. | CaH2是还原剂 |
6.能正确表示下列化学反应的离子方程式的是( )
| A. | 碳酸钠溶于足量盐酸中 Na2CO3+2H+=2Na++CO2↑+H2O | |
| B. | 氧化钠与稀硫酸的反应 Na2O+2H+=2Na++H2O | |
| C. | 氢氧化钡溶液与硫酸铜溶液反应 Ba2++SO42-=BaSO4↓ | |
| D. | 铁片插入稀硫酸溶液中 Fe+2H+=Fe3++H2↑ |