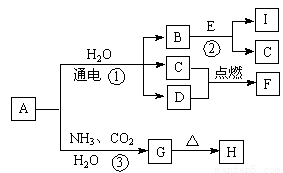
题目内容
亚铁是血红蛋白重要组成成分,起着向人体组织传送O2的作用,如果缺铁就可能出现缺铁性贫血,但是摄入过量的铁也有害。下面是一种常见补药品说明书中的部分内容:该药品含Fe2+33%~36%,不溶于水但能溶于人体中的胃酸:与Vc(维生素C)同服可增加本品吸收。
(一)甲同学设计了以下下实验检测该补铁药品中是否含有Fe2+并探究Vc的作用:

(1)加入新制氯水后溶液中发生的离子反应方程式是_________________________、
Fe3+ +SCN- [Fe(SCN) ]2+ 。
[Fe(SCN) ]2+ 。
(2)加入KSCN溶液后溶液变为淡红色,说明溶液中有少量Fe3+。该离子存在的原因可能是(填编号)_____________________。
A.药品中的铁本来就应该以三价铁的形式存在
B.在制药过程中生成少量三价铁
C.药品储存过程中有少量三价铁生成
(3)药品说明书中“与Vc同服可增加本品吸收”请说明理由_______________________。
(二)乙同学采用在酸性条件下用高锰酸钾标准溶液滴定的方法测定该药品是否合格,反应原理为 。准确称量上述药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
。准确称量上述药品10.00g,将其全部溶于试剂2中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。
(4)该实验中的试剂2与甲同学设计的实验中的试剂1都可以是______(填序号)。
A.蒸馏水B.稀盐酸C.稀硫酸D.稀硝酸
(5)本实验滴定过程中操作滴定管的图示正确的是_______(填编号)。

(6)请通过计算,说明该药品含“铁”量是否合格(写出主要计算过程)?
(1)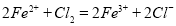 (2)B、C
(2)B、C
(3)Fe2+在人体血红蛋白中起传送O2的作用,Fe3+没有此功能,服用Vc可防止药品中的Fe2+被氧化成Fe3+(或答人体只能吸收Fe2+,Fe2+在人体血红蛋白中起传送O2的作用,服用Vc可防止药品中的Fe2+被氧化成Fe3+)(其他合理答案也可给分)。
(4)C(5)A
(6)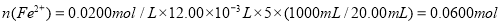
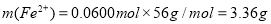
含“铁”量为: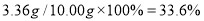 ,该药品含“铁”量合格。(分步适当给分)
,该药品含“铁”量合格。(分步适当给分)
【解析】
试题分析:(一)(1)根据题给信息和流程图知,加入新制氯水后溶液变血红色,Fe2+被氧化成Fe3+,发生的离子反应方程式是Cl2 + 2Fe2+=2Fe3+ + 2Cl-、Fe3+ +SCN- [Fe(SCN) ]2+ ;(2)加入KSCN溶液后溶液变为淡红色,说明溶液中有少量Fe3+。A.根据题给信息知药品中的铁应该以二价铁的形式存在,错误;B.二价铁具有较强的还原性,在制药过程中可能被空气中的氧气氧化生成少量三价铁,正确;C.二价铁具有较强的还原性,药品储存过程中可能被空气中的氧气氧化生成少量三价铁,正确,选BC;(3)由题给信息知,Vc具有还原性,Fe2+在人体血红蛋白中起传送O2的作用,Fe3+没有此功能,服用Vc可防止药品中的Fe2+被氧化成Fe3+(或答人体只能吸收Fe2+,Fe2+在人体血红蛋白中起传送O2的作用,服用Vc可防止药品中的Fe2+被氧化成Fe3+);(二)(4)根据题给信息知,该药片可溶于酸,而盐酸可与高锰酸钾标准溶液发生氧化还原反应,稀硝酸具有强氧化性,能将Fe2+氧化成Fe3+,故选用稀硫酸,选C;(5)本实验滴定过程中用到高锰酸钾标准溶液具有强氧化性,应用酸式滴定管盛装,滴定时应左手控制活塞,右手摇动锥形瓶,操作滴定管的图示正确的是A;(6)根据题给化学方程式得关系式:5Fe2+——MnO4—,则
[Fe(SCN) ]2+ ;(2)加入KSCN溶液后溶液变为淡红色,说明溶液中有少量Fe3+。A.根据题给信息知药品中的铁应该以二价铁的形式存在,错误;B.二价铁具有较强的还原性,在制药过程中可能被空气中的氧气氧化生成少量三价铁,正确;C.二价铁具有较强的还原性,药品储存过程中可能被空气中的氧气氧化生成少量三价铁,正确,选BC;(3)由题给信息知,Vc具有还原性,Fe2+在人体血红蛋白中起传送O2的作用,Fe3+没有此功能,服用Vc可防止药品中的Fe2+被氧化成Fe3+(或答人体只能吸收Fe2+,Fe2+在人体血红蛋白中起传送O2的作用,服用Vc可防止药品中的Fe2+被氧化成Fe3+);(二)(4)根据题给信息知,该药片可溶于酸,而盐酸可与高锰酸钾标准溶液发生氧化还原反应,稀硝酸具有强氧化性,能将Fe2+氧化成Fe3+,故选用稀硫酸,选C;(5)本实验滴定过程中用到高锰酸钾标准溶液具有强氧化性,应用酸式滴定管盛装,滴定时应左手控制活塞,右手摇动锥形瓶,操作滴定管的图示正确的是A;(6)根据题给化学方程式得关系式:5Fe2+——MnO4—,则
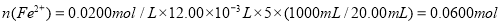 ,
,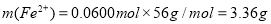 ,含“铁”量为:
,含“铁”量为: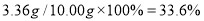 ,该药品含“铁”量合格。
,该药品含“铁”量合格。
考点:考查离子方程式的书写、铁元素化合物的性质就、氧化还原滴定及关系式法计算,考查阅读材料接受信息的能力、灵活运用所学知识的能力。

在10 L的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下表:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答:
(1)该反应为 (填“吸热”或“放热”)反应。
(2)该反应的化学平衡常数表达式为K = 。
(3)能说明该反应达到化学平衡状态的是 (填字母)。
a.υ正(CO2)=υ正(H2) b.υ逆(CO)=υ逆(H2O)
c.υ逆(H2)=υ逆(H2O) d.υ正(H2)=υ逆(H2)
(4)某温度下,将CO2和H2各0.10 mol充入该容器中,达到平衡后,测得 c(CO)=0.0080 mol·L-1 ,则CO2的转化率为 。
(5)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。