题目内容
【题目】已知:① A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平 ② ![]() 。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
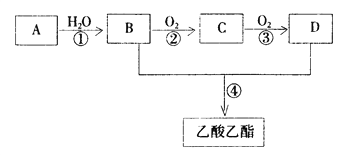
回答下列问题:
(1)B、D分子中的官能团名称分别是 __________、___________。
(2)写出下列反应的反应类型:①__________,②__________,④________。
(3)写出下列反应的化学方程式:
②____________________________;④_____________________________。
【答案】 羟基 羧基 加成 氧化 取代(酯化) ![]()
![]()
![]()
![]()
【解析】A的产量通常衡量一个国家的石油化工水平,则A应为CH2=CH2,与水在一定条件下发生加成反应生成CH3CH2OH,乙醇在Cu或Ag作催化剂条件下发生氧化反应CH3CHO,CH3CHO可进一步氧化物CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成乙酸乙酯,另外乙烯中含有C=C,在一定条件下发生加聚反应生成![]() ,则A为CH2=CH2,B为CH3CH2OH,C为CH3CHO,D为CH3COOH。(2)B为CH3CH2OH,D为CH3COOH,分别含有的官能团为羟基和羧基;(2)反应①A为CH2=CH2,与水在一定条件下发生加成反应生成CH3CH2OH,反应②是CH3CH2OH在Cu或Ag作催化剂、加热条件下发生氧化反应生成CH3CHO,反应④是乙醇与乙酸在浓硫酸、加热条件下发生酯化反应生成乙酸乙酯;(3)反应②是CH3CH2OH在Cu或Ag作催化剂、加热条件下发生氧化反应生成CH3CHO,其化学方程式为:
,则A为CH2=CH2,B为CH3CH2OH,C为CH3CHO,D为CH3COOH。(2)B为CH3CH2OH,D为CH3COOH,分别含有的官能团为羟基和羧基;(2)反应①A为CH2=CH2,与水在一定条件下发生加成反应生成CH3CH2OH,反应②是CH3CH2OH在Cu或Ag作催化剂、加热条件下发生氧化反应生成CH3CHO,反应④是乙醇与乙酸在浓硫酸、加热条件下发生酯化反应生成乙酸乙酯;(3)反应②是CH3CH2OH在Cu或Ag作催化剂、加热条件下发生氧化反应生成CH3CHO,其化学方程式为:![]() ;反应④是乙醇与乙酸在浓硫酸、加热条件下发生酯化反应生成乙酸乙酯,其化学方程式为:
;反应④是乙醇与乙酸在浓硫酸、加热条件下发生酯化反应生成乙酸乙酯,其化学方程式为:![]()
![]()
![]() 。
。

练习册系列答案
相关题目