题目内容
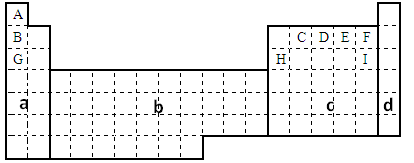
a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构示意图为 ,b与c形成的化合物的电子式为
,b与c形成的化合物的电子式为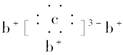 。下列说法中正确的是( )
。下列说法中正确的是( )
 ,b与c形成的化合物的电子式为
,b与c形成的化合物的电子式为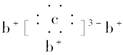 。下列说法中正确的是( )
。下列说法中正确的是( )| A.原子半径:a>c>d>b | B.电负性:a>b>d>c |
| C.原子序数:d>a>c>b | D.最高价含氧酸的酸性:c>d>a |
D
根据原子核外电子的排布规律可知,K层只能容纳2个电子,所以x=2,即a是硅元素,。根据b与c形成的化合物的化学式可知,b是第IA,c是第ⅤA,所以b是钠,d是磷元素,则C是氮元素。所以原子半径是b>a>d>c,非金属性越强,电负性越大,因此电负性是c>d>a>b。原子序数为d>a>b>c,非金属性越强,最高价氧化物的水化物的酸性越强,所以选项D是正确的,答案选D。

练习册系列答案
相关题目