题目内容
(10分)五种元素的原子电子层结构如下:
(1)元素的第一电离能最大的是 ;
(2)属于过渡元素的是 ;
(3)元素的电负性最大的是 ;
(4)上述元素之间能形成X2Y型化合物的化学式是 、
| A.1s22s1; | B.1s22s22p4; | C.1s22s22p6; | D.1s22s22p63s23p2 E.[Ar]3d104s1。(用元素符号作答) |
(2)属于过渡元素的是 ;
(3)元素的电负性最大的是 ;
(4)上述元素之间能形成X2Y型化合物的化学式是 、
(各2分,共10分)(1)Ne (2)Cu (3)O (4)Li2O Cu2O
根据原子的核外电子排布式可知,A是Li,B是O,C是Ne,D是Si,E是Cu。
(1)稀有气体元素的最外层已经达到8电子稳定结构,第一电离能最大。
(2)周期表中第3列到第12列共计10列元素,全部属于金属元素,属于过渡元素,因此是铜。
(3)非金属性越强,电负性越大,所以是氧元素。
(4)根据元素的化合价可知,化学式为Li2O、Cu2O。
(1)稀有气体元素的最外层已经达到8电子稳定结构,第一电离能最大。
(2)周期表中第3列到第12列共计10列元素,全部属于金属元素,属于过渡元素,因此是铜。
(3)非金属性越强,电负性越大,所以是氧元素。
(4)根据元素的化合价可知,化学式为Li2O、Cu2O。

练习册系列答案
相关题目
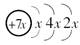 ,b与c形成的化合物的电子式为
,b与c形成的化合物的电子式为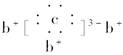 。下列说法中正确的是( )
。下列说法中正确的是( )