题目内容
【题目】流动电池可以在电池外部调节电解质溶液,从而维持电池内部电解质溶液浓度稳定,原理如图。下列说法不正确的是
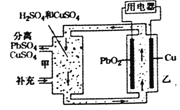
A. 甲中应补充硫酸
B. 当消耗1molPbO2时需分离出1molCuSO4
C. 电子由PbO2极流出经过用电器流向Cu极
D. 电池总反应为:Cu+PbO2+2H2SO4=CuSO4+PbSO4+2H2O
【答案】C
【解析】电池的两个电极是Cu和PbO2,金属单质为负极,所以Cu为负极,反应为:Cu-2e-=Cu2+,PbO2为正极,反应为:PbO2 + 4H+ + 2e- = Pb2+ + 2H2O,总反应为:Cu+PbO2+2H2SO4=CuSO4+PbSO4+2H2O。随着反应的进行硫酸逐渐转化为硫酸铜和硫酸铅,所以需要不断补充硫酸,选项A正确。根据方程式,每消耗1molPbO2时应该生成1mol硫酸铜,所以需要分离出去的就是1mol硫酸铜。(图中甲装置上标注了硫酸和硫酸铜,可能是该装置的初始电解液是硫酸和硫酸铜的混合溶液,反应中需要的分离的是新生成的硫酸铜和硫酸铅)选项B正确。电子应该有负极流出,流向正极,题目中Cu为负极,选项C错误。由上,电池的总反应为:Cu+PbO2+2H2SO4=CuSO4+PbSO4+2H2O。选项D正确。

练习册系列答案
相关题目