题目内容
13.下面是四个化学反应,你认为理论上不可用于设计原电池的化学反应是( )| A. | Zn+Ag2O+H2O═Zn(OH)2+2Ag | B. | Pb+PbO2+2H2SO4═2PbSO4+2H2O | ||
| C. | Zn+CuSO4═Cu+ZnSO4 | D. | CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3 |
分析 自发的氧化还原反应能设计成原电池.
解答 解:A、属于氧化还原反应,能用于设计原电池,故A不选;
B、属于氧化还原反应,能设计成原电池,故B不选;
C、属于自发的氧化还原反应,能设计成原电池,故C不选;
D、不属于自发的氧化还原反应,不能设计成原电池,故D选.
故选D.
点评 本题考查学生设计成原电池的反应具备的条件,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
8.某无色水溶液中能大量共存的离子组是( )
| A. | K+、Na+、CO32-、Cl- | B. | Ca2+、K+、CO32-、OH- | ||
| C. | Fe3+、Ba2+、NO3-、SO4- | D. | H+、Na+、HCO3-、OH- |
9.以下叙述中错误的是( )
| A. | 钠和氯气反应生成食盐后,其结构的稳定性增强 | |
| B. | 离子化合物不一定都易溶于水 | |
| C. | 任何离子键在形成的过程中必定有电子的得与失 | |
| D. | 钠和氧气反应生成过氧化钠后,体系的能量降低 |
5.可用于干燥NH3的试剂是( )
| A. | 无水CaCl2 | B. | 浓H2SO4 | C. | P2O5 | D. | 碱石灰 |
2.乙烯的产量是衡量一个国家石油化工生产水平的标志,这是由于乙烯在石油化工生产中具有广泛的用途.下列关于乙烯的用途叙述不正确的是( )
| A. | 以乙烯为原料可以合成聚乙烯等制备生活用品的材料 | |
| B. | 乙烯可以用来制备1,2-二氯乙烷(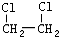 ) ) | |
| C. | 乙烯可以与水发生加成反应制备乙醇(CH3CH2OH) | |
| D. | 乙烯可以与Br2发生加成反应制备二溴乙烷(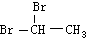 ) ) |
3.下列实验可行的是( )
| A. | 用酸性高锰酸钾溶液除去乙烷中的乙烯 | |
| B. | 用苯与浓溴水在FeBr3催化作用下制溴苯 | |
| C. | 用食醋浸泡有水垢的水壶清除其中的水垢 | |
| D. | 用乙醇从碘水中萃取碘 |
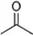 根据键线式回答下列问题:
根据键线式回答下列问题: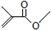 分子式:C5H8O2,
分子式:C5H8O2,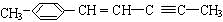 分子中最多有4个原子共直线;
分子中最多有4个原子共直线;
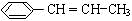 )在催化剂作用下生成聚苯丙烯的反应方程式:
)在催化剂作用下生成聚苯丙烯的反应方程式: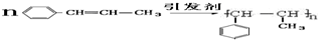 .
.