题目内容
3.下列实验可行的是( )| A. | 用酸性高锰酸钾溶液除去乙烷中的乙烯 | |
| B. | 用苯与浓溴水在FeBr3催化作用下制溴苯 | |
| C. | 用食醋浸泡有水垢的水壶清除其中的水垢 | |
| D. | 用乙醇从碘水中萃取碘 |
分析 A.烯被酸性高锰酸钾氧化生成二氧化碳气体;
B.苯和液溴在FeBr3作催化剂条件下制取溴苯;
C.水垢的成分是碳酸钙和氢氧化镁,能和醋酸反应;
D.乙醇易溶和碘水混溶不能萃取.
解答 解:A.烯被酸性高锰酸钾氧化生成二氧化碳气体,引入新杂质,应用溴水除杂,故A错误;
B.苯和液溴在FeBr3作催化剂条件下制取溴苯,苯和浓溴水不反应,故B错误;
C.醋酸和水垢中的碳酸钙和氢氧化镁反应生成了溶于水的盐,除去水垢,故C正确;
D.萃取是利用物质在两种互不相溶的溶剂中的溶解度不同,从一种溶剂中转移到另一种溶剂中,再利用分液、蒸馏的方法进行分离,乙醇与水溶液混溶,不分层,故D错误.
故选C.
点评 本题综合考查物质的制备、分离提纯、除杂问题,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意把握物质的性质的异同,把握实验方法和注意事项,难度不大.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
13.下面是四个化学反应,你认为理论上不可用于设计原电池的化学反应是( )
| A. | Zn+Ag2O+H2O═Zn(OH)2+2Ag | B. | Pb+PbO2+2H2SO4═2PbSO4+2H2O | ||
| C. | Zn+CuSO4═Cu+ZnSO4 | D. | CaO+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3 |
14.15g物质A和10.5g物质B完全反应,生成7.2g物质C、1.8g物质D和标准状况下6.72L的气态物质E,则物质E的摩尔质量是( )
| A. | 16.5 g/mol | B. | 85 g/mol | C. | 55 g/mol | D. | 27.5 g/mol |
11. 霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物,结构简式如下.下列关于MMF说法中不正确的是( )
霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物,结构简式如下.下列关于MMF说法中不正确的是( )
 霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物,结构简式如下.下列关于MMF说法中不正确的是( )
霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物,结构简式如下.下列关于MMF说法中不正确的是( )| A. | MMF既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2反应发生取代 | |
| B. | 1molMMF能与含3molNaOH的水溶液完全反应 | |
| C. | MMF即可以催化加氢,又可以使酸性高锰酸钾溶液褪色 | |
| D. | MMF既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2 |
8.下列说法正确的是( )
| A. | 焓变是指1mol物质完全参加反应时的能量变化 | |
| B. | 中和滴定实验时,用待测液润洗锥形瓶 | |
| C. | 已知:2HI(g)?H2(g)+I2(g)△H=8.8kJ•mol-1,若向密闭容器中充入1molHI(g),则分解过程中吸收的热量为4.4kJ | |
| D. | 对于反应3H2(g)+N2(g)?2NH3(g),若使用催化剂,v正、v逆同等程度加快 |
15.下列物质不能与二氧化硅发生化学反应的是( )
| A. | CaO | B. | 氢氟酸 | C. | NaOH溶液 | D. | 浓硫酸 |
12.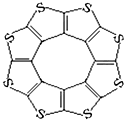 最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图所示),每个平面上下两侧最多可储存10个H2分子.
最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图所示),每个平面上下两侧最多可储存10个H2分子.
①元素电负性大小关系是:C<S(填“>”、“=”或“<”).
②分子中C原子的杂化轨道类型为sp2.
③有关键长数据如下:
从表中数据可以看出,C16S8中碳硫键键长介于C-S与C=S之间,原因可能是:分子中的C与S原子之间有π键或分子中的碳硫键具有一定程度的双键性质.
④C16S8与H2微粒间的作用力是范德华力.
 最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图所示),每个平面上下两侧最多可储存10个H2分子.
最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图所示),每个平面上下两侧最多可储存10个H2分子.①元素电负性大小关系是:C<S(填“>”、“=”或“<”).
②分子中C原子的杂化轨道类型为sp2.
③有关键长数据如下:
| C-S | C=S | C16S8中碳硫键 | |
| 键长/pm | 181 | 155 | 176 |
④C16S8与H2微粒间的作用力是范德华力.
