题目内容
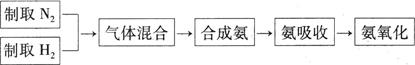
(16分)实验室模拟合成氨和氨催化氧化的流程如下:
已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。

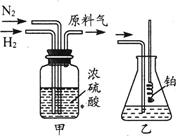
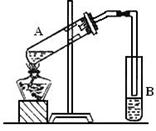
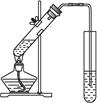
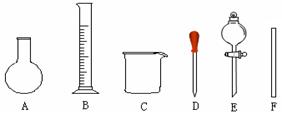
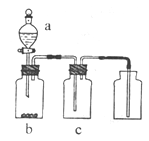
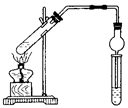
(1)从图中选择制取气体的合适装置:氮气和氢气分别为 和 。
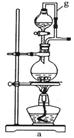
(2)装置a中g管的作用是 ;
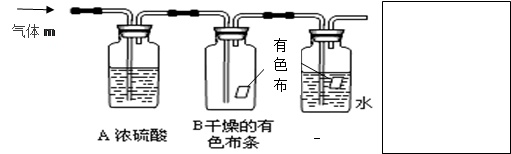
(3)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有
的作用。
(4)氨合成器出来经冷却的气体持续通入乙装置的水中吸收氨, (填“会”或“不会”)发生倒吸,原因是 。
(5)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是 ,锥形瓶中还可观察到的现象是 。
(6)写出乙装置中氨氧化的化学方程式: 。

已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。



(1)从图中选择制取气体的合适装置:氮气和氢气分别为 和 。
(2)装置a中g管的作用是 ;
(3)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有
的作用。
(4)氨合成器出来经冷却的气体持续通入乙装置的水中吸收氨, (填“会”或“不会”)发生倒吸,原因是 。
(5)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是 ,锥形瓶中还可观察到的现象是 。
(6)写出乙装置中氨氧化的化学方程式: 。
(1)a和b (2)平衡压强 (3)干燥气体控制氢气和氮气的流速
(4)不会 因为混合气体中含有大量难溶于水的氮、氢两种气体
(5)说明氨的氧化反应是一个放热反应 有红棕色气体产生(白烟等)
(6)4NH3+5O2 4NO+6H2O
4NO+6H2O
(4)不会 因为混合气体中含有大量难溶于水的氮、氢两种气体
(5)说明氨的氧化反应是一个放热反应 有红棕色气体产生(白烟等)
(6)4NH3+5O2
 4NO+6H2O
4NO+6H2O(1)根据题意可知制取氮气属于液体和液体反应且需要加热的,所以选择装置a。实验室制取氢气属于固体和液体之间的反应,但不需要加热,所以选择b装置。
(2)装置a中在反应过程中压强比较大,为了使液体顺利从分液漏斗中滴下,需要平衡内
外压强,使其相等。
(3)因为氨气的合成是可逆反应,所以为了控制反应速率可以通过气泡的快慢来调节反应
速率,同时浓硫酸具有吸水性,可以干燥氮气和氢气。
(4)虽然氨气极易溶于水,但反应是可逆反应,生成的氨气中含有大量难溶于水的氨气和氢气,所以不会发生倒吸。
(5)能使铂丝保持红热,说明反应是放热反应,放出的热量足以维持反应继续进行。氨气被氧化生成物是NO,但NO易被空气氧化生成红棕色的NO2气体。
(2)装置a中在反应过程中压强比较大,为了使液体顺利从分液漏斗中滴下,需要平衡内
外压强,使其相等。
(3)因为氨气的合成是可逆反应,所以为了控制反应速率可以通过气泡的快慢来调节反应
速率,同时浓硫酸具有吸水性,可以干燥氮气和氢气。
(4)虽然氨气极易溶于水,但反应是可逆反应,生成的氨气中含有大量难溶于水的氨气和氢气,所以不会发生倒吸。
(5)能使铂丝保持红热,说明反应是放热反应,放出的热量足以维持反应继续进行。氨气被氧化生成物是NO,但NO易被空气氧化生成红棕色的NO2气体。

练习册系列答案
相关题目