题目内容
下列各组气体中,在通常状况下能共存,并且都能用浓硫酸干燥的是
| A.SO2、H2S、Cl2 | B.SO2、O2、NH3 |
| C.SO2、CO2、O2 | D.HCl、H2S、HI |
C
A中三者不能共存(因:SO2+2H2S=3S+2H2O H2S+Cl2=S+2HCl),且H2S不能用浓硫酸干燥(因H2S具还原性,浓硫酸有强氧化性,所以H2S能被浓硫酸氧化);
B中SO2、NH3不能共存(因两者能发生反应),NH3不能用浓硫酸干燥(因2NH3+H2SO4=(NH4)2SO4);
D中三者能共存,但H2S、HI不能用浓硫酸干燥(原因同A,发生氧化还原反应);
B中SO2、NH3不能共存(因两者能发生反应),NH3不能用浓硫酸干燥(因2NH3+H2SO4=(NH4)2SO4);
D中三者能共存,但H2S、HI不能用浓硫酸干燥(原因同A,发生氧化还原反应);

练习册系列答案
相关题目


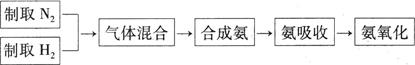

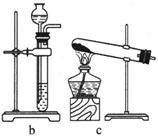

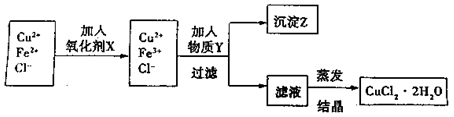
 始沉淀时的pH
始沉淀时的pH 。(填序号)
。(填序号) ++H2↑设计实验来制取CuCl2溶液,该同学设计的装置应该为 。(填“原电池”或“电解池”)
++H2↑设计实验来制取CuCl2溶液,该同学设计的装置应该为 。(填“原电池”或“电解池”)