题目内容
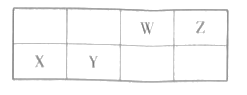
【题目】下表列出了①~⑥六种元素在周期表中的位置:
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ |
(1)⑤元素的原子结构示意图为_____________;
(2)③元素原子的最外层电子数为___________;
(3)⑤元素与④元素形成的离子化合物的化学式为_________(写出一种即可);
(4)②、③、④三种元素的非金属性逐渐___________(填“减弱”或“增强”);
(5)④元素和⑥元素形成的氢化物,其稳定性的强弱顺序为_______>_______(填化学式)。
【答案】![]() 5 Na2O或Na2O2 增强 H2O H2S
5 Na2O或Na2O2 增强 H2O H2S
【解析】
由元素在周期表中的位置可知,①为H、②为C、③为N、④为O、⑤为Na、⑥为S,根据此分析进行解答。
(1)⑤为Na,原子结构示意图为![]() 。
。
故答案为 ![]()
(2)③为N,原子序数为7,最外层电子数为5.
故答案为 5
(3)④为O、⑤为Na,组合出的离子化合物为Na2O或Na2O2。
故答案为 Na2O或Na2O2
(4)同周期,原子序数依次增大,自左而右元素非金属性增强。
故答案为 增强
(5)④为O、⑥为S氢化物分别为水和硫化氢,且O的非金属性强于S,故稳定性的强弱顺序为H2O>H2S。
故答案为 H2O H2S

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目