题目内容
15.中和4g某NaOH的溶液,用去盐酸25mL,求该盐酸的浓度.分析 根据n=$\frac{m}{M}$计算NaOH的物质的量,由方程式计算HCl的物质的量,再根据c=$\frac{n}{V}$计算.
解答 解:氢氧化钠的物质的量n=$\frac{m}{M}$=$\frac{4g}{40g/mol}$=0.1mol,
由方程式HCl+NaOH=NaCl+H2O可知,n(HCl)=n(NaOH)=0.1mol,
HCl溶液中溶质的物质的量浓度=$\frac{n}{V}$=$\frac{0.1mol}{0.025L}$=4mol/L
答:该盐酸的浓度为4mol/L.
点评 本题考查了物质的量的有关计算,题目难度不大,注意掌握有关的计算公式,侧重于基础知识的考查.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.下面是实验室可制取氨气的装置和选用的试剂,其中正确的是( )
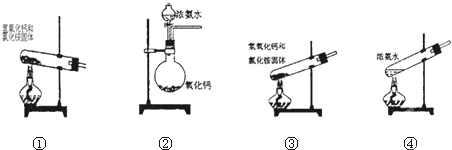

| A. | ①②④ | B. | 只有④ | C. | ①② | D. | 只有③ |
6.下列各组离子能在强酸性的溶液中大量共存,且溶液呈无色的是( )
| A. | K+、Na+、MnO4-、SO42- | B. | K+、Na+、CO32-、Cl- | ||
| C. | Mg2+、NH4+、Cl-、NO3- | D. | Ba2+、K+、OH-、SO42- |
4.分子式为 C8H10的苯的同系物,其苯环上的一氯代物的种类有( )
| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
5. 科学家最近合成了一种烃,根据分析,绘制出了该烃分子的球棍模型(如图),关于该烃的下列说法正确的是( )
科学家最近合成了一种烃,根据分析,绘制出了该烃分子的球棍模型(如图),关于该烃的下列说法正确的是( )
 科学家最近合成了一种烃,根据分析,绘制出了该烃分子的球棍模型(如图),关于该烃的下列说法正确的是( )
科学家最近合成了一种烃,根据分析,绘制出了该烃分子的球棍模型(如图),关于该烃的下列说法正确的是( )| A. | 分子中碳原子所处的位置都相同 | |
| B. | 该烃分子中含有极性键,故易溶于水 | |
| C. | 该烃的一卤代物只有一种结构 | |
| D. | 分子中只有C-C单键,没有C=C双键 |

 )是比较简单的稠环芳香烃.请回答以下问题:
)是比较简单的稠环芳香烃.请回答以下问题: ;
;