��Ŀ����
����Ŀ����֪Ca3(PO4)2��SiO2��C���¹��ȿ��Է�Ӧ�õ�CaSiO3��P4������CO����Ӧ���£�Ca3(PO4)2+SiO2+C![]() CaSiO3+P4��+CO����
CaSiO3+P4��+CO����
��1����ƽ�÷�Ӧ����ʽ�����������ת�Ʒ������Ŀ_____��
��2���÷�Ӧ�б���ԭ��Ԫ����___������������______��
��3��ÿ����24.0g̼ʱ����___�����ӷ���ת�ƣ�����P4__g��
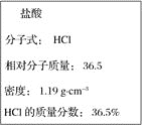
��4����Ӧ���û�����壬����ɱ���£��������ܶ�Ϊ____g/L��������λС������
��5����÷�Ӧ���漰������Ԫ����ͬ����ĵ�Ԫ�أ������ˮ�帻Ӫ��������Ҫԭ����ij��ˮ��NH4Cl����Ϊ180 mg/L��
��д��NH4Cl�ĵ���ʽ____��
��Ϊ��ȥ��ˮ�е�NH4+����103L����ˮ�м���0.1 mol/LNaOH��Һ���������·�Ӧ��NH4++OH-=NH3+H2O������������ҪNaOH��Һ�����Ϊ___L��������������λС������
���𰸡�
![]() CO 4NA 24.8 1.64
CO 4NA 24.8 1.64 ![]() 33.64
33.64
��������
��1�����û��ϼ���������ƽ��
��2����Ӧ������������ԭ�����ϼ۽��ͣ���ԭ�������������������
��3������������ԭ��Ӧ�е�ʧ�����غ���㣻
��4������![]() =m/V���㣻
=m/V���㣻
��5����NH4ClΪ���ӻ������笠����ӡ������ӹ��ɣ�
�ڸ��ݷ���ʽ���㡣
��1����Ӧ��C�Ļ��ϼ���0�۱�Ϊ+2�ۣ�P�Ļ��ϼ���+5��Ϊ0�ۣ�����P4��������4��P���뷴Ӧ������С������Ϊ20��ת��20�����ӣ���Ca3(PO4)2��ϵ��Ϊ2��P4ϵ��Ϊ1��C��CO��ϵ��Ϊ10������ԭ���غ㣬SiO2ϵ��Ϊ6������ʽ������ת�Ʒ���Ϊ ��
��
��2����Ӧ������������ԭ�����ϼ۽��ͣ���ԭ��Ԫ��Ϊ![]() ����ԭ�������������������ΪCO��
����ԭ�������������������ΪCO��
��3��ÿ����24.0g̼ʱ����2mol��ת��4mol���ӣ�����0.2mol P4����24.8g��
��4��ÿ����24.0g̼ʱ������2molCO��0.2mol P4��������������Ϊ56+24.8=80.8g������µ����Ϊ2.2![]() 22.4=49.28L���ܶ�=80.8g/49.28L=1.64g/L��
22.4=49.28L���ܶ�=80.8g/49.28L=1.64g/L��
��5����NH4ClΪ���ӻ������笠����ӡ������ӹ��ɣ������ʽΪ![]() ��
��
��180 mg/L![]() 103L=180g��n��NH4Cl��=180g/53.5g/mol=3.364mol�����ݷ���ʽ��n��NH4Cl��= n��NaOH��=0.1 mol/L
103L=180g��n��NH4Cl��=180g/53.5g/mol=3.364mol�����ݷ���ʽ��n��NH4Cl��= n��NaOH��=0.1 mol/L![]() V����V=33.64L��
V����V=33.64L��