题目内容
4.下列说法正确的是( )| A. | 明矾净水过程中不涉及化学变化 | |
| B. | 由同种元素组成的物质一定是纯净物 | |
| C. | 风化、石油分馏和碘的升华都是物理变化 | |
| D. | 为除去蛋白质溶液中少量的NaCl,可以利用渗析的方法 |
分析 A.有新物质生成的是化学变化;
B.同素异形体混合,是由同种元素组成的混合物;
C.结晶水合物在常温和较干燥的空气里失去部分或全部结晶水的现象叫风化;
D.蛋白质溶液是胶体.
解答 解:A.明矾净水原理是明矾中的铝离子先发生水解生成氢氧化铝胶体,胶体具有吸附作用,可用来净水.明矾水解生成胶体过程属于化学变化,故A错误;
B.同种元素组成的物质不一定是纯净物,如氧气和臭氧,故B错误;
C.风化是化学变化,故C错误;
D.蛋白质粒子直径在1nm~100nm之间,为中性胶体,粒子不带电荷,能透过滤纸,但不能透过半透膜,食盐溶液中钠离子和氯离子粒子直径小于1nm,能透过半透膜,可用渗析的方法分离,故D正确.
故选D.
点评 本题考查物理变化、化学变化的区别和纯净物以及胶体的性质等,难度不大,注意风化是化学变化.

练习册系列答案
相关题目
12. 单质硼有无定形和晶体两种,参考下表数据
单质硼有无定形和晶体两种,参考下表数据
(1)晶体硼的晶体类型属于原子晶体,理由是熔、沸点很高、硬度很大.
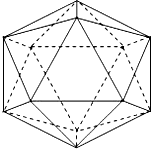
(2)已知晶体硼结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个项点上各有1个B原子.通过视察图形及推算,此晶体体结构单元由12个硼原子构成.其中B-B键的键角为60°.共含有30个B-B.
 单质硼有无定形和晶体两种,参考下表数据
单质硼有无定形和晶体两种,参考下表数据| 金刚石 | 晶体硅 | 晶体硼 | |
| 熔点 | 3823 | 1683 | 2573 |
| 沸点 | 5100 | 2628 | 2823 |
| 硬度 | 10 | 7.0 | 9.5 |
(2)已知晶体硼结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个项点上各有1个B原子.通过视察图形及推算,此晶体体结构单元由12个硼原子构成.其中B-B键的键角为60°.共含有30个B-B.
16.日前中国量子物质科学协同创新中心的江颖课题组和王恩哥课题组合作,在水科学领域取得重大突破,在国际上首次实现了水分子的亚分子级分辨成像,使得解析水的氢键网络构型成为可能.(图a是实验器件示意图,图b是拍摄到的图片的一部分,图c是图b所对应的结构示意图)下列有关说法不正确的是( )
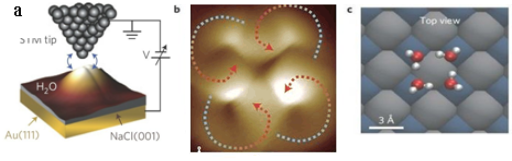

| A. | 图a所示实验器件中,用氯化钠作为绝缘薄膜层,是因为氯化钠晶体不导电 | |
| B. | 图b是表示一个H2O分子内部的氢键和氢氧共价键结构特征示意图 | |
| C. | 水分子间形成氢键使水的熔点和沸点升高 | |
| D. | H2O分子的稳定性很强,是因为分子内氢氧共价键强 |
13.下列物质中,既能跟盐酸反应,又能跟氢氧化钠溶液反应的化合物是( )
| A. | Na2CO3 | B. | Na2SO4 | C. | Al2O3 | D. | Al |
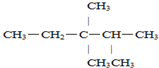 2,3,3-三甲基戊烷;
2,3,3-三甲基戊烷;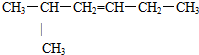 2-甲基-3-己烯;
2-甲基-3-己烯;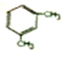 1,3-二甲基苯.(用系统命名法命名)
1,3-二甲基苯.(用系统命名法命名)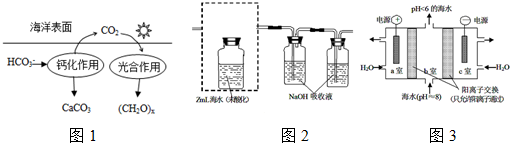
 A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题: