��Ŀ����
ij�������ﺬNH4I��NaHCO3��AlCl3��MgBr2��FeCl2�еļ���,Ϊȷ���ù�������ijɷּ�����ɳɷֵ����ʵ���֮��,�ֽ�������ʵ�顣
ʵ���:

(1)��ɫ����Ϊ ��
(2)�ù�������ijɷ�Ϊ ��
ʵ���:ȡһ�����ĸù�����������ˮ���1 L��Һ,����û����Һ��ͨ��һ������Cl2,�����Һ�м���������(�ֱ���A-��B-��C-��ʾ)�����ʵ�����ͨ��Cl2����Ĺ�ϵ�����ʾ��
Cl2����� (��״����)/L | 2.8 | 5.6 | 11.2 |
n(A-)/mol | 1.25 | 1.5 | 2 |
n(B-)/mol | 1.5 | 1.4 | 0.9 |
n(C-)/mol | a | 0 | 0 |
(3)a= ��
(4)ԭ���������и���ɳɷֵ����ʵ���֮��Ϊ ��
(1)NH3
(2)NH4I��MgBr2��AlCl3
(3)0.15
(4)n(AlCl3)��n(MgBr2)��n(NH4I)=20��45��24
��������(1)�������NaOH��Һ������,���ɵ���ɫ����ֻ����NH3,˵��һ������NH4I��
(2)���ɰ�ɫ�����Ҿ����ޱ仯,˵��һ����FeCl2��һ����MgBr2;������ɫ��Һ������ϡ�������ɫ����,�ӹ���ϡ����������ܽ�,�����ݲ���,�Ƴ���AlCl3��NaHCO3��(3)�ɱ�������֪,A-ΪCl-��B-ΪBr-��C-ΪI-,�Ƚ�ͨ�� 5.6 L ��2.8 L��״����Cl2����Һ�����ӵı仯�����֪:��ͨ��2.8 L Cl2,��0.125 mol Cl2,���Cl-����0.25 mol, Br-����0.1 mol,I-����a mol,���ݷ�Ӧ��ϵʽ:
Cl2 �� 2Br- , Cl2 �� 2I-
1 2 1 2
0.05 mol 0.1 mol (0.125-0.05)mol a mol
�ɵ�a=0.15
(4)������֪,ԭ�����Һ��n(Cl-)=1.25 mol-0.125 mol��2=1 mol,n(Br-)=1.5 mol,n(I-)=0.15 mol+0.125 mol��2=0.4 mol����n(AlCl3)��n(MgBr2)��n(NH4I)=[n(Cl-)/3]��[n(Br-)/2]��n(I-)=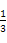 mol��
mol��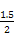 mol��0.4 mol=20��45��24��
mol��0.4 mol=20��45��24��

 ��У����ϵ�д�
��У����ϵ�д�