题目内容
将一定质量的镁、铜合金加入到稀硝酸溶液中,两者恰好完全反应,假设反应过程中还原产物全部是NO,向所得溶液中加入物质的量浓度为3 mol·L-1的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g,则下列有关叙述中正确的是( )
A.开始加入合金的质量可能为16.4 g
B.参加反应的硝酸的物质的量为0.1 mol
C.生成沉淀完全时消耗NaOH溶液的体积为100 mL
D.标准状况下产物NO的体积为22.4 L
C
【解析】合金增加的质量即为OH-的质量,则n(OH-)=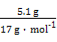 =0.3 mol,
=0.3 mol,
V(NaOH溶液)= =0.1 L,即为100 mL,C对;根据电子守恒和电荷守恒可知,反应中转移的电子为0.3 mol。若全部为Mg,质量为3.6 g,若全部是铜,质量为9.6 g,A错;被还原的硝酸为0.1 mol,起酸性作用的硝酸为0.3 mol,B错;标准状况下产物NO的体积为2.24 L,D错。
=0.1 L,即为100 mL,C对;根据电子守恒和电荷守恒可知,反应中转移的电子为0.3 mol。若全部为Mg,质量为3.6 g,若全部是铜,质量为9.6 g,A错;被还原的硝酸为0.1 mol,起酸性作用的硝酸为0.3 mol,B错;标准状况下产物NO的体积为2.24 L,D错。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案某固体混合物含NH4I、NaHCO3、AlCl3、MgBr2、FeCl2中的几种,为确定该固体混合物的成分及各组成成分的物质的量之比,现进行如下实验。
实验Ⅰ:

(1)无色气体为 。
(2)该固体混合物的成分为 。
实验Ⅱ:取一定量的该固体混合物溶于水配成1 L溶液,并向该混合溶液中通入一定量的Cl2,测得溶液中几种阴离子(分别用A-、B-、C-表示)的物质的量与通入Cl2体积的关系如表所示。
Cl2的体积 (标准状况下)/L | 2.8 | 5.6 | 11.2 |
n(A-)/mol | 1.25 | 1.5 | 2 |
n(B-)/mol | 1.5 | 1.4 | 0.9 |
n(C-)/mol | a | 0 | 0 |
(3)a= 。
(4)原固体混合物中各组成成分的物质的量之比为 。