题目内容
15.把铁片放入下列溶液中,铁片溶解,溶液质量增加,但没有气体放出的是( )| A. | 稀HNO3 | B. | CuSO4溶液 | C. | FeCl3溶液 | D. | AgNO3溶液 |
分析 铁和溶液中的溶质反应,导致铁片溶解,溶液质量增加且没有气体生成,说明铁和溶液反应时不是和酸反应,且不能置换出比铁的摩尔质量大的金属单质,据此解答.
解答 解:A.铁与稀硝酸反应生成一氧化氮气体,不符合题意,故A不选;
B.铁与硫酸铜反应生成铜和硫酸亚铁溶液,溶液质量增加,故B不选;
C.铁与氯化铁反应生成氯化亚铁,铁溶解,溶液质量增加,故C选;
D.铁与硝酸银反应生成银和硝酸亚铁,溶液质量增加,故D不选;
故选:C.
点评 本题考查铁的化学性质,注意探究与铁反应后溶液质量增减的问题,根据与铁反应前后溶质的相对分子质量的大小来确定溶液质量的增减即可,难度不大.

练习册系列答案
相关题目
5.过氧化钙难溶于水,溶于酸生成过氧化氢,在医药上用作杀菌剂、防腐剂等.
Ⅰ.某小组用含有少量氧化亚铁和氧化铁杂质的大理石制取过氧化钙的流程如下:
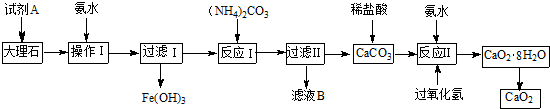
请回答下列问题:
(1)操作I的目的是调节溶液的pH,使铁元素完全沉淀,则试剂A最好选用c.
a.盐酸 b.硝酸 c.盐酸和过氧化氢 d.硫酸
(2)检验操作I中铁元素已沉淀完全的操作是取上层清液少许于试管中,滴加KSCN溶液,若溶液不变红,则铁元素已除净.
(3)滤液B主要成分的化学式是NH4Cl.
(4)反应Ⅱ是放热反应.保持H2O2物质的量一定,当H2O2浓度小于20%时,CaO2的产率随H2O2浓度的增大而增大;但浓度大于20%后,CaO2产率反而下降.试分析CaO2产率下降的可能原因是H2O2浓度高,反应速率快,反应放热使体系升温迅速,促使H2O2分解.
Ⅱ.过氧化钙中常含有CaO杂质,实验室可按以下步骤测定CaO2含量:
步骤1:准确称取0.3900g过氧化钙样品,置于250mL的锥形瓶中;
步骤2:分别加入10mL蒸馏水和20mL磷酸(1:3),振荡使样品完全溶解;
步骤3:用0.1000mol•L-1 KMnO4标准溶液滴定至终点,记录数据;
步骤4:平行测定4次(数据记录见下表),计算试样中CaO2的质量分数.
已知:上述实验过程中反应关系为:CaO2~H2O2,5H2O2~2KMnO4
请回答下列问题:
(5)步骤3判断滴定达到终点的现象是当看到加入1滴KMnO4溶液,锥形瓶中溶液由无色变为浅红色(或粉红色、红色),30s不褪色,即达到滴定终点;
(6)由表中数据可知,该样品中CaO2含量为90%.若实验时刚洗净的滴定管未用KMnO4标准溶液润洗,则CaO2的质量分数测定结果偏高(填“偏高”、“偏低”或“无影响”).
Ⅰ.某小组用含有少量氧化亚铁和氧化铁杂质的大理石制取过氧化钙的流程如下:

请回答下列问题:
(1)操作I的目的是调节溶液的pH,使铁元素完全沉淀,则试剂A最好选用c.
a.盐酸 b.硝酸 c.盐酸和过氧化氢 d.硫酸
(2)检验操作I中铁元素已沉淀完全的操作是取上层清液少许于试管中,滴加KSCN溶液,若溶液不变红,则铁元素已除净.
(3)滤液B主要成分的化学式是NH4Cl.
(4)反应Ⅱ是放热反应.保持H2O2物质的量一定,当H2O2浓度小于20%时,CaO2的产率随H2O2浓度的增大而增大;但浓度大于20%后,CaO2产率反而下降.试分析CaO2产率下降的可能原因是H2O2浓度高,反应速率快,反应放热使体系升温迅速,促使H2O2分解.
Ⅱ.过氧化钙中常含有CaO杂质,实验室可按以下步骤测定CaO2含量:
步骤1:准确称取0.3900g过氧化钙样品,置于250mL的锥形瓶中;
步骤2:分别加入10mL蒸馏水和20mL磷酸(1:3),振荡使样品完全溶解;
步骤3:用0.1000mol•L-1 KMnO4标准溶液滴定至终点,记录数据;
步骤4:平行测定4次(数据记录见下表),计算试样中CaO2的质量分数.
| 实验 | 1 | 2 | 3 | 4 |
| V(KMnO4)/mL | 19.50 | 21.50 | 19.48 | 19.52 |
请回答下列问题:
(5)步骤3判断滴定达到终点的现象是当看到加入1滴KMnO4溶液,锥形瓶中溶液由无色变为浅红色(或粉红色、红色),30s不褪色,即达到滴定终点;
(6)由表中数据可知,该样品中CaO2含量为90%.若实验时刚洗净的滴定管未用KMnO4标准溶液润洗,则CaO2的质量分数测定结果偏高(填“偏高”、“偏低”或“无影响”).
6.下列说法正确的是( )
| A. | 化学反应不一定有分子碰撞 | B. | 化学反应的活化能一定大于零 | ||
| C. | 具有较高能量的分子是活化分子 | D. | 发生有效碰撞的分子是活化分子 |
3.A、B、C、D、E均为短周期元素,且原子序数依次增大,请根据表中信息回答下列问题:
(1)E在元素周期表中的位置第三周期第ⅥA族.
(2)B最简单气态氢化物的电子式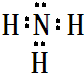 ,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式
,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式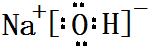 ,所含化学键类型:离子键、共价键.
,所含化学键类型:离子键、共价键.
(3)B、C、D、E简单离子半径由大到小顺序为:S2->N3->O2->Na+(填元素符号).
(4)用电子式表示E的氢化物的形成过程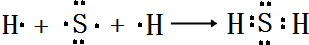 .
.
(5)由A、B、C与氢元素组成的一种常见酸式盐与过量D的最高价氧化物的水化物反应的离子方程式:NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O.
(6)19.2g金属铜与一定浓度的B的最高价氧化物的水化物反应,产生标准状况下NO、NO2(不考虑N2O4的存在)混合气6.72L,则参加反应的HNO3的物质的量为0.9mol.
| 元素 | 元素性质或结构 |
| A | 最外层电子数是其内层电子数的2倍 |
| B | B元素的单质在空气中含量最多 |
| C | C元素在地壳中含量最多 |
| D | D元素在同周期中金属性最强 |
| E | 常温常压下,E元素形成的单质是淡黄色固体,常在火山口附近沉积 |
(2)B最简单气态氢化物的电子式
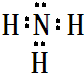 ,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式
,属于共价化合物(填“离子”或“共价”);D的最高价氧化物的水化物电子式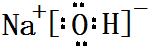 ,所含化学键类型:离子键、共价键.
,所含化学键类型:离子键、共价键.(3)B、C、D、E简单离子半径由大到小顺序为:S2->N3->O2->Na+(填元素符号).
(4)用电子式表示E的氢化物的形成过程
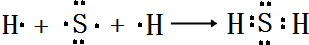 .
.(5)由A、B、C与氢元素组成的一种常见酸式盐与过量D的最高价氧化物的水化物反应的离子方程式:NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O.
(6)19.2g金属铜与一定浓度的B的最高价氧化物的水化物反应,产生标准状况下NO、NO2(不考虑N2O4的存在)混合气6.72L,则参加反应的HNO3的物质的量为0.9mol.
10.有a g氧化铜和氧化铁的混合物,加入2mol•L-1的稀硫酸溶液50mL,恰好完全溶解,若将a g该混合物在过量的CO气流中加热充分反应,冷却后剩余固体的质量为( )
| A. | 1.6a g | B. | (a-1.6)g | C. | (a-3.2)g | D. | 无法计算 |
20.下列各种叙述中,正确的是( )
①Cl-和Cl2的性质相同 ②ClO-具有氧化性 ③Cl-比Cl多一个电子 ④盐酸兼有酸性、氧化性、还原性 ⑤Cl-具有酸性 ⑥Cl2的氧化性比MnO2的强 ⑦Cl2只有氧化性而没有还原性.
①Cl-和Cl2的性质相同 ②ClO-具有氧化性 ③Cl-比Cl多一个电子 ④盐酸兼有酸性、氧化性、还原性 ⑤Cl-具有酸性 ⑥Cl2的氧化性比MnO2的强 ⑦Cl2只有氧化性而没有还原性.
| A. | ①②⑤⑥ | B. | 仅②④⑥ | C. | 仅②③④ | D. | ②③④⑥ |
7.下列变化不属于氮的固定的是( )
| A. | 根瘤菌把氮气转化为氨 | B. | 氮气和氢气在适宜条件下合成氨 | ||
| C. | 氮气和氧气在放电条件下合成NO | D. | 工业上用氨和二氧化碳合成尿素 |
5.下列反应中,调节反应物用量或浓度不会改变反应产物的是( )
| A. | CO2 通入澄清石灰水中 | B. | Na2CO3溶液和HCl溶液反应 | ||
| C. | AlCl3溶液的NaOH 溶液反应 | D. | 铁丝在氯气中燃烧 |
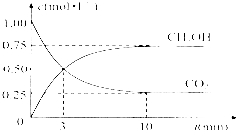 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.