题目内容
某温度下,在一密闭容器中发生如下可逆反应:2E(g)?F(g)+xG(g);△H<0.若起始时E浓度为a mol?L-1,F、G浓度均为0,达平衡时E浓度为O.5a mol?L-1;若E的起始浓度改为 2a mol?L-1,F、G浓度仍为O,当达到新的平衡时,下列说法正确的是( )A.升高温度时,正反应速率加快、逆反应速率减慢
B.若x=l,容器体积保持不变,新平衡下E的体积分数为50%
C.若x=2,容器体积保持不变,新平衡下F的平衡浓度小于0.5a mol?L-1
D.若x=2,容器压强保持不变,新平衡下E的物质的量为a mol
【答案】分析:A、升高温度正、逆反应速率都增大;
B、容器体积保持不变,x=l,反应前后气体的物质的量不变,若E的起始浓度改为 2a mol?L-1,等效为增大压强,平衡不移动,新平衡下E的体积分数与原平衡相等;
C、容器体积保持不变,若E的起始浓度改为 2a mol?L-1,等效为在原平衡的基础上增大2mol/LE的浓度,反应向正反应进行,F的浓度增大;
D、题目中为物质的量的浓度,不能确定物质具体物质的量.
解答:解:A、升高温度正、逆反应速率都增大,故A错误;
B、容器体积保持不变,x=l,反应前后气体的物质的量不变,若E的起始浓度改为 2a mol?L-1,等效为增大压强,平衡不移动,平衡时E的转化率不变,新平衡下E的体积分数与原平衡相等为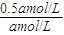 ×100%=50%,故B正确;
×100%=50%,故B正确;
C、原平衡时E浓度为O.5a mol?L-1,△c(E)=a mol?L-1-O.5a mol?L-1=O.5a mol?L-1,故平衡时F的浓度为O.5a mol?L-1,容器体积保持不变,若E的起始浓度改为 2a mol?L-1,等效为在原平衡的基础上增大2mol/LE的浓度,反应向正反应进行,F的浓度增大,故大于O.5a mol?L-1,故C错误;
D、容器压强保持不变,若E的起始浓度改为 2a mol?L-1,与原平衡为等效平衡,E的转化率相同,平衡时E的物质的量为原平衡的2倍,题目中为物质的量的浓度,不能确定物质的量,原平衡E的物质的量不一定是0.5amol,故D错误;
故选B.
点评:考查化学平衡的计算、平衡状态的构建与等效平衡等,难度中等,设计平衡状态建立的途径是关键,注意等效思想的运用.
B、容器体积保持不变,x=l,反应前后气体的物质的量不变,若E的起始浓度改为 2a mol?L-1,等效为增大压强,平衡不移动,新平衡下E的体积分数与原平衡相等;
C、容器体积保持不变,若E的起始浓度改为 2a mol?L-1,等效为在原平衡的基础上增大2mol/LE的浓度,反应向正反应进行,F的浓度增大;
D、题目中为物质的量的浓度,不能确定物质具体物质的量.
解答:解:A、升高温度正、逆反应速率都增大,故A错误;
B、容器体积保持不变,x=l,反应前后气体的物质的量不变,若E的起始浓度改为 2a mol?L-1,等效为增大压强,平衡不移动,平衡时E的转化率不变,新平衡下E的体积分数与原平衡相等为
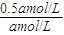 ×100%=50%,故B正确;
×100%=50%,故B正确;C、原平衡时E浓度为O.5a mol?L-1,△c(E)=a mol?L-1-O.5a mol?L-1=O.5a mol?L-1,故平衡时F的浓度为O.5a mol?L-1,容器体积保持不变,若E的起始浓度改为 2a mol?L-1,等效为在原平衡的基础上增大2mol/LE的浓度,反应向正反应进行,F的浓度增大,故大于O.5a mol?L-1,故C错误;
D、容器压强保持不变,若E的起始浓度改为 2a mol?L-1,与原平衡为等效平衡,E的转化率相同,平衡时E的物质的量为原平衡的2倍,题目中为物质的量的浓度,不能确定物质的量,原平衡E的物质的量不一定是0.5amol,故D错误;
故选B.
点评:考查化学平衡的计算、平衡状态的构建与等效平衡等,难度中等,设计平衡状态建立的途径是关键,注意等效思想的运用.

练习册系列答案
相关题目
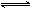 2C(g)+D(g),达平衡后A的转化率为x.
2C(g)+D(g),达平衡后A的转化率为x.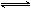 2C(g)+D(g),达平衡后A的转化率为x.
2C(g)+D(g),达平衡后A的转化率为x. C(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )
C(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表,下列说法正确的是( )


 mol;
mol;

 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)