题目内容
【题目】某溶液只含下表离子中的几种,且各离子的物质的量浓度相等(不考虑水的电离与离子水解)。
阳离子 | K+、NH4+、Fe2+、Mg2+、Cu2+ |
阴离子 | OH-、Cl-、CO32-、SO42- |
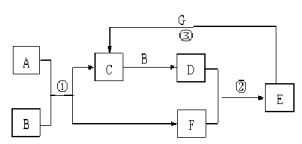
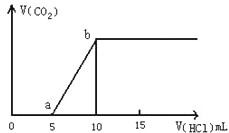
某同学进行了如下实验(必要时可加热):

下列说法正确的是
A. 由沉淀A推断原溶液中一定含有SO42-
B. 原溶液中只含有NH4+、Fe2+、Cl-、SO42-
C. 滤液A中可能含有K+
D. 沉淀B中一定含有Mg(OH)2
【答案】B
【解析】试题分析:某溶液只含下表离子中的几种,且各离子的物质的量浓度相等,向试液中加入过量稀硫酸,无明显现象,说明没有CO32-,在加入硝酸钡溶液,产生气体A,沉淀A,说明溶液中含有Fe2+,Fe2+、NO3-和H+能发生氧化还原反应生成Fe3+、NO和水,气体A为NO,溶液中不含OH-和CO32-,沉淀A是硫酸钡,稀硫酸和硝酸钡反应可生成硫酸钡,所以由沉淀A无法推断原溶液中是否含有SO42-,再向滤液中加热NaOH溶液,产生气体B,在碱性溶液中能生成气体的只有NH4+,则气体A为NH3,沉淀B为Fe(OH)3,向滤液B中加入少量CO2产生白色沉淀C,沉淀C为BaCO3,根据电荷守恒,溶液中的阴离子有Cl-、SO42-,综上所述,原溶液中只含有NH4+、Fe2+、Cl-、SO42-,答案选B。

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目