题目内容
12. 化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题.
化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题.(1)已知:C(s)+O2(g)═CO2(g)△H1=-396.5kJ•mol-1;
H2(g)+$\frac{1}{2}$O2═H2O(g)△H2=-241.8kJ•mol-1;
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H3=-283.0kJ•mol-1.
根据盖斯定律写出单质碳和水蒸气生成水煤气的热化学方程式:C(s)+H2O(g)=CO(g)+H2(g)△H=+128.3 kJ•mol-1;
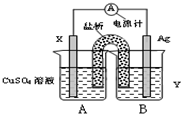
(2)依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s) 设计的双液原电池,可以提供稳定的电流.装置如图所示,其中盐桥中装有琼脂-饱和KCl溶液.
回答下列问题:
①电极X的材料和电解质溶液Y分别为Cu、AgNO3溶液;
②盐桥中K+移向B(填A或B);
③银电极发生的电极反应为Ag++e-=Ag.
分析 (1)①C(s)+O2(g)=CO2(g)△H1=-396.5kJ•mol-1
②H2(g)+1/2O2=H2O(g)△H2=-241.8kJ•mol-1
③CO(g)+1/2O2(g)=CO2(g)△H3=-283.0kJ•mol-1
根据盖斯定律,①-②-③计算得到;
(2)①在原电池中,活泼失电子的金属为负极,得电子的阳离子是电解质中的阳离子;
②依据原电池的电极反应和溶液中的电荷守恒分析判断离子移动方向;
③依据银电极做原电池的正极,在电极上是溶液中银离子得到电子发生还原反应.
解答 解:(1)①C(s)+O2(g)=CO2(g)△H1=-396.5kJ•mol-1
②H2(g)+1/2O2=H2O(g)△H2=-241.8kJ•mol-1
③CO(g)+1/2O2(g)=CO2(g)△H3=-283.0kJ•mol-1
根据盖斯定律,①-②-③得到:单质碳和水蒸气生成水煤气的热化学方程式:C(s)+H2O(g)=CO(g)+H2(g)△H=128.3 kJ•mol-1
故答案为:C(s)+H2O(g)=CO(g)+H2(g)△H=+128.3 kJ•mol-1;
(2)①氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)中,活泼的失电子的金属Cu为负极,得电子的阳离子Ag+是电解质中的阳离子,所以电解质可以选择AgNO3溶液;故答案为:Cu、AgNO3溶液;
②原电池反应,B池中Ag+析出,为符合溶液的电中性,盐桥中的钾离子移向B池;故答案为:B;
③银电极发生的电极反应为溶液中的银离子得到电子析出银单质,电极反应为:Ag++e-=Ag,故答案为:Ag++e-=Ag.
点评 本题考查学生原电池的设计、构成条件以及工作原理知识,盖斯定律的计算应用,注意知识的积累是解题关键,难度中等.

| A. | 容器中混合气体的平均相对分子质量增大 | |
| B. | 正反应速率增大,逆反应速率减小,平衡向正反应方向移动 | |
| C. | 正反应速率和逆反应速率都变小,C的百分含量增加 | |
| D. | 混合气体密度的变化情况不可以作为判断反应是否再次达平衡的依据 |
| A. | 工业上制取Y的单质常用还原剂还原Y的氧化物 | |
| B. | Z的最高价氧化物能与水反应生成相应的酸 | |
| C. | 室温下,X的最高价氧化物的水溶液的pH>7 | |
| D. | Y单质在一定条件下可以与氧化铁发生置换反应 |
| A. | ClO-做还原剂 | |
| B. | 制备1molK2FeO4时转移3mol 电子 | |
| C. | 高铁酸钾中铁的化合价为+7 | |
| D. | Fe(OH)3在反应中被还原,发生还原反应 |
 一块表面被氧化的铝分成两等分,若向其中一份中滴加1mol•L-1的NaOH溶液,向另一份中滴加x mol•L-1的稀盐酸,产生氢气的物质的量与所加NaOH溶液、稀盐酸的体积关系如图所示.下列说法不正确的是( )
一块表面被氧化的铝分成两等分,若向其中一份中滴加1mol•L-1的NaOH溶液,向另一份中滴加x mol•L-1的稀盐酸,产生氢气的物质的量与所加NaOH溶液、稀盐酸的体积关系如图所示.下列说法不正确的是( )| A. | 该铝块的总质量为8.46g | |
| B. | a=260 | |
| C. | b=780 | |
| D. | 该铝块中氧化铝与铝单质的物质的量之比为3:20 |
 铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等.回答下列问题:
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等.回答下列问题: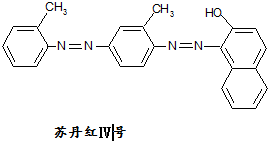 据2006年11月12 中央电视台每周质量报告报道,北京市场上销售的一部分标称是白洋淀特产的“红心鸭蛋”含偶氮染料“苏丹红Ⅳ号”,国际癌症研究机构将其列为三类致癌物.
据2006年11月12 中央电视台每周质量报告报道,北京市场上销售的一部分标称是白洋淀特产的“红心鸭蛋”含偶氮染料“苏丹红Ⅳ号”,国际癌症研究机构将其列为三类致癌物.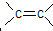 空间结构,且是不能旋转不然,双键就会被破坏,而单键是可以旋转的,则肯定共线的原子最多有12个.
空间结构,且是不能旋转不然,双键就会被破坏,而单键是可以旋转的,则肯定共线的原子最多有12个. )在碱性条件下水解的装置图。进行皂化反应时的步骤如下:
)在碱性条件下水解的装置图。进行皂化反应时的步骤如下:
 g氢氧化钠,5 mL水和10 mL酒精。加入酒精的作用是____________。
g氢氧化钠,5 mL水和10 mL酒精。加入酒精的作用是____________。 3)图中长玻璃导管的作用为_________________________。
3)图中长玻璃导管的作用为_________________________。