题目内容
【题目】常温下,用![]() 溶液分别滴定浓度均为
溶液分别滴定浓度均为![]() 的
的![]() 、
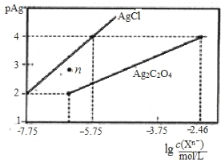
、![]() 溶液,所得的沉淀溶解平衡图像如图所示(不考虑
溶液,所得的沉淀溶解平衡图像如图所示(不考虑![]() 的水解,
的水解,![]() ),下列说法正确的是( )
),下列说法正确的是( )
A.![]() 的数量级等于
的数量级等于![]()
B.n点表示![]() 的不饱和溶液
的不饱和溶液
C.向![]() 的混合液中滴入
的混合液中滴入![]() 溶液时,先生成
溶液时,先生成![]() 沉淀
沉淀
D.![]() 的平衡常数为
的平衡常数为![]()
【答案】D
【解析】
A.根据图象,当![]() =4,即
=4,即![]() 时,c(
时,c(![]() )=
)=![]() mol/L,
mol/L,![]() ,数量级为10-11,故A错误;
,数量级为10-11,故A错误;
B.在n点,c(Ag+)大于平衡浓度,故n点的浓度积Qc(AgCl)>Ksp(AgCl),为氯化银的过饱和溶液,将有沉淀析出,故B错误;
C.根据图象可知,当阴离子浓度相同时,生成AgCl沉淀所需的c(Ag+)小,因此向![]() 的混合液中滴入AgNO3溶液时,先析出氯化银沉淀,故C错误;
的混合液中滴入AgNO3溶液时,先析出氯化银沉淀,故C错误;
D.![]() 的平衡常数K=
的平衡常数K=![]() ,此时溶液中的c(Ag+)相同,故有:K=
,此时溶液中的c(Ag+)相同,故有:K=![]() =
=![]()
![]() ,故D正确;
,故D正确;
故选D。

【题目】下列除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)( )
选项 | 物质 | 选用的试剂 | 操作方法 |
A | NaCl(泥沙) | 水 | 过滤 |
B | CO2(CO) | O2 | 点燃 |
C | Fe(Zn) | 稀硫酸 | 结晶 |
D | CO2(HCl) | NaOH溶液 | 洗气 |
A.AB.BC.CD.D
【题目】向2L密闭容器中加入1molNO和1mol活性炭,发生反应:2NO(g)+C(s) ![]() N2(g)+CO2(g) △H = -213.5kJ/mol,达到平衡的数据如下:
N2(g)+CO2(g) △H = -213.5kJ/mol,达到平衡的数据如下:
温度/℃ | n(活性炭)/mol | n(CO2)/mol |
T1 | 0.70 | —— |
T2 | —— | 0.25 |
下列说法不正确的是( )
A. 上述信息可推知:T1<T2
B. T1℃时,该反应的平衡常数K=9/16
C. T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小
D. T2℃时,若反应达平衡后再缩小容器的体积。c(N2)/c(NO)不变
【题目】汽车尾气中含有CO、NO等有害气体。
(1)汽车尾气中NO生成过程的能量变化示意图如图该条件下,1molN2和1molO2完全反应生成NO会吸收______kJ能量。

(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
实验编号 | t(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.2×10-3 | 5.80×10-3 | 82 |
Ⅱ | 280 | 1.2×10-3 | b | 124 |
Ⅲ | 350 | a | 5.80×10-3 | 82 |
①请表中数据补充完整:a___________;b___________。
②能验证温度对化学反应速率规律的是实验________![]() 填实验序号
填实验序号![]() 。
。
(3)在2L密闭容器内,800℃时反应:2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) |
|
|
|
|
|
|
①用![]() 表示从0-2s内该反应的平均速率
表示从0-2s内该反应的平均速率![]() ______。
______。
②能说明该反应已达到平衡状态的是______
a.单位时间内消耗nmol![]() 的同时,生成2nmol
的同时,生成2nmol![]()
b.容器内各物质的浓度保持不变
c. 2v逆(NO)=v正(O2)
d.混合气体的总物质的量不随时间的变化而变化