题目内容
12.氮元素的单质和化合物在化工、农业生产中用途广泛.下列有关氮及其化合物的性质中:(1)常用作食品袋中填充气的是N2(填化学式);常用作制冷剂的化合物是NH3
(填化学式);该物质在空气中与HCl相遇有白烟现象,产生该现象的化学反应方程式是NH3+HCl=NH4Cl.
(2)汽车燃料中一般不含氮元素,但尾气却所含有NO,产生的原因用化学方程式表示N2+O2$\frac{\underline{\;高温\;}}{\;}$2NO.
(3)NO对大气的影响之一是导致酸雨,用化学方程式表示NO形成酸雨的原因是2NO+O2═2NO2、3NO2+H2O═2HNO3+NO.
分析 (1)氮气化学性质稳定,常用作食品袋中填充气,氨气易液化,属于碱性气体,易和氯化氢反应;
(2)空气中的氮气在放电或高温下反应生成NO;
(3)NO与空气的主要成份氧气反应生成二氧化氮,二氧化氮与水反应生成硝酸和一氧化氮.
解答 解:(1)N2化学性质稳定,常用作食品袋中填充气,NH3易液化,常作制冷剂,氨气属于碱性气体,易和氯化氢反应生成氯化铵,即NH3+HCl=NH4Cl,
故答案为:N2;NH3;NH3+HCl=NH4Cl;
(2)空气中的氮气在放电或高温下反应生成NO,该反应为N2+O2$\frac{\underline{\;高温\;}}{\;}$2NO,
故答案为:N2+O2$\frac{\underline{\;高温\;}}{\;}$2NO;
(3)NO与空气的主要成份氧气反应生成二氧化氮,反应方程式为:2NO+O2═2NO2,二氧化氮与水反应生成硝酸和一氧化氮,反应方程式为:3NO2+H2O═2HNO3+NO,所以NO对大气的影响之一是导致酸雨,
故答案为:2NO+O2═2NO2、3NO2+H2O═2HNO3+NO.
点评 本题考查学生含氮元素物质的性质以及应用知识,注意知识的归纳和梳理是解题的关键,题目难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
2.下列关于水玻璃的性质和用途的叙述中正确的是( )
| A. | 它是一种纯净物,既不燃烧也不易腐蚀 | |
| B. | 水玻璃是生产玻璃的主要原料之一 | |
| C. | 木柴、织物浸过水玻璃具有防腐性能且不易燃烧 | |
| D. | 水玻璃的化学性质稳定,在空气中不易变质 |
7.物质的量浓度相同的三种正盐NaX、NaY、NaZ的水溶液,其pH分别为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是( )
| A. | HX,HZ,HY | B. | HX,HY,HZ | C. | HZ,HY,HX | D. | HY,HZ,HX |
17.将下列物质按酸、碱、盐分类排列,正确的是( )
| A. | 硫酸、纯碱、硫酸钙 | B. | 盐酸、苛性钠、硫酸亚铁 | ||
| C. | 碳酸、乙醇、烧碱 | D. | 磷酸、熟石灰、生石灰 |
4.下列叙述正确的是( )
| A. | 蔗糖与浓硫酸反应中有海绵状的炭生成,是因为浓硫酸具有吸水性能使蔗糖炭化 | |
| B. | 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体,体现浓硫酸的强氧化性 | |
| C. | 浓硫酸是一种干燥剂,能够干燥硫化氢、氢气等气体 | |
| D. | 浓硫酸在常温下可用铁桶盛装,是因为常温下浓硫酸能够使铁、铝等金属钝化 |
1.下列化学用语使用正确的是( )
| A. | 葡萄糖、淀粉的最简式都是CH2O | B. | CH4的电子式是 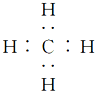 | ||
| C. | 乙醛分子的结构简式是CH3COH | D. | 丙烷分子的球棍模型是 |
2.下列实验操作中有错误的是( )
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,温度计水银球应浸没在液体中 | |
| C. | 蒸馏中,冷却水应从冷凝管的下口通入,上口流出 | |
| D. | 把几滴FeCl3饱和溶液滴入250mL沸水中继续煮沸至红褐色制取Fe(OH)3胶体 |