题目内容
【题目】CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
已知反应Fe(s)+CO2(g)![]() FeO(s)+CO(g)的平衡常数为K1;
FeO(s)+CO(g)的平衡常数为K1;
反应Fe(s)+H2O(g)![]() FeO(s)+H2(g)的平衡常数为K2。
FeO(s)+H2(g)的平衡常数为K2。
在不同温度时K1、K2的值如下表:
温度(绝对温度) | K1 | K2 |
973 | 1.47 | 2.38 |
1173 | 2.15 | 1.67 |
(1)推导反应CO2(g)+H2(g)![]() CO(g)+H2O(g)的平衡常数K与K1、K2的关系式:_____________________。
CO(g)+H2O(g)的平衡常数K与K1、K2的关系式:_____________________。
(2)通过K值的计算,(1)中的反应是_________反应(填“吸热”或“放热”)。
(3)在一体积为10L的密闭容器中,加入一定量的CO2和H2O(g),在1173开时发生反应并记录前5min的浓度,第6min时改变了反应的条件。各物质的浓度变化如下表:
时间/min | CO2 | H2O | CO | H2 |
0 | 0.2000 | 0.3000 | 0 | 0 |
2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | |
5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
6 | 0.0350 | 0.1350 | 0.1650 |
①前2min,用CO表示的该化学反应的速率是:_______________________。
②在3~4min之间,反应处于___________状态(填“平衡”或“非平衡”)。
③第6min时,平衡向_________方向移动,可能的原因是______________________。
【答案】K=![]() 吸热 v(CO)=0.0130mol·L-1·nin-1 平衡 右或正反应 升高温度或降低了H2浓度
吸热 v(CO)=0.0130mol·L-1·nin-1 平衡 右或正反应 升高温度或降低了H2浓度
【解析】
(1) 利用盖斯定律计算平衡常数K、K1与K2之间的关系式;
(2)根据温度升高平衡常数的变化判断,由表中数据知升温平衡常数变大,说明平衡正向移动;
(3) ①根据v=![]() 计算;
计算;
②根据可逆反应特征:可逆反应到达平衡时,各组分的浓度保持不变;
③6min时,CO2浓度降低、H2O的浓度减小、CO的浓度增大,平衡正向移动,可能是改变温度或移走水蒸气。
(1)CO2(g)+H2(g)![]() CO(g)+H2O(g)平衡常数K的表达式K=
CO(g)+H2O(g)平衡常数K的表达式K= ![]() ;
;
Fe(s)+CO2(g)![]() FeO(s)+CO(g)的平衡常数为K1=
FeO(s)+CO(g)的平衡常数为K1=![]() ;
;
Fe(s)+H2O(g)![]() FeO(s)+H2(g)的平衡常数为K2=
FeO(s)+H2(g)的平衡常数为K2=![]() ,由平衡常数分析计算可知,K与K1、K2二者的关系为K=
,由平衡常数分析计算可知,K与K1、K2二者的关系为K=![]() ;
;
(2)973时,K=![]() =
=![]() =0.68;1173时,K=
=0.68;1173时,K=![]() =
=![]() =1.43;故升高温度,K值增大,平衡正向移动,(1)中的反应是吸热反应;
=1.43;故升高温度,K值增大,平衡正向移动,(1)中的反应是吸热反应;
(3)①前2min,用CO表示的该化学反应的速率c(CO)= =0.013mol/(Lmin);
=0.013mol/(Lmin);
②由表中数据可知,3min、 4min时, 反应混合物对应物质的浓度不变,处于与平衡状态;
③表6min时, CO2浓度降低、H2O的浓度减小、CO的浓度增大,说明平衡向正反应移动,正反应为吸热反应,可能是升高温度,由于氢气物质的量未知,也可能是降低氢气浓度。

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案【题目】氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
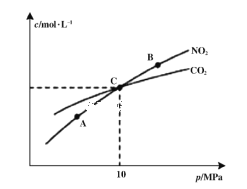
(1)根据如图提供的信息,写出该反应的热化学方程式____________________________,下图的曲线中________(填“a” 或“b”)表示加入铁触媒(催化剂)的能量变化曲线。
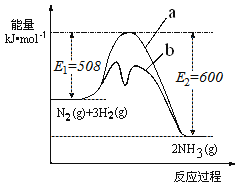
(2)在恒容容器中,下列描述中能说明上述反应已达平衡的是_____________。
A.3υ(H2)正=2υ(NH3)逆
B.单位时间内生成n molN2的同时生成2n molNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
(3)500℃、50MPa时,在容积为1 L的容器中加入1 mol N2、3 mol H2,反应达平衡后测得平衡常数为K,此时N2的转化率为a。则K和a的关系是K=_______________。
(4)为了寻找合成NH3的适宜条件,某同学设计了三组实验(如下表),请在下表空格处填入相应的实验条件及数据。
实验编号 | T(℃) | n (N2)/n(H2) | P(MPa) |
ⅰ | 450 |
| 1 |
ⅱ | ______ |
| 10 |
ⅲ | 480 | ______ | 10 |
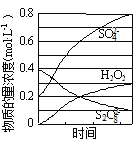
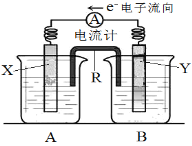
(5)1998年希腊亚里斯多德大学的两位科学家采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电解合成氨。其实验装置如图。阴极的电极反应式为________________________。
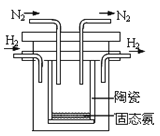
【题目】实验室用绿矾(FeSO4·7H2O)为原料制备补血剂甘氨酸亚铁[(H2NCH2COO)2Fe],有关物质性质如下:
甘氨酸(H2NCH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有酸性和还原性 | 易溶于水,难溶于乙醇 |
实验过程:
I.配制含0.10molFeSO4的绿矾溶液。
II.制备FeCO3:向配制好的绿矾溶液中,缓慢加入200mL1.1mol/LNH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀。
III.制备(H2NCH2COO)2Fe:实验装置如下图(夹持和加热仪器已省略),将实验II得到的沉淀和含0.20mol甘氨酸的水溶液混合后加入C中,然后利用A中反应产生的气体将C中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。
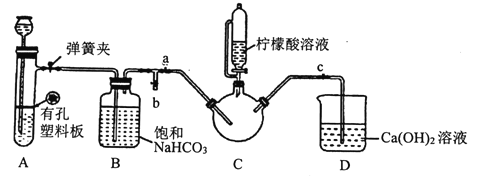
回答下列问题:
(1)实验I中:实验室配制绿矾溶液时,为防止FeSO4被氧化变质,应加入的试剂为____(写化学式)。
(2)实验II中:生成沉淀的离子方程式为________________。
(3)实验III中:
①检查装置A的气密性的方法是_________。
②装置A中所盛放的药品是_______ (填序号)。
a.Na2CO3和稀H2SO4 b.CaCO3和稀H2SO4 c.CaCO3和稀盐酸
③确认c中空气排尽的实验现象是______________。
④加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是_______。
⑤洗涤实验III中得到的沉淀,所选用的最佳洗涤试剂是___(填序号)。
a.热水 b.乙醇溶液 c.柠檬酸溶液
⑥若产品的质量为17.34g,则产率为_____。