题目内容
【题目】双氧水是常见的氧化剂、消毒剂,一种制取双氧水的流程如下:
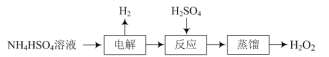
(1)“电解”后生成(NH4)2S2O8,该反应的化学方程式为______。
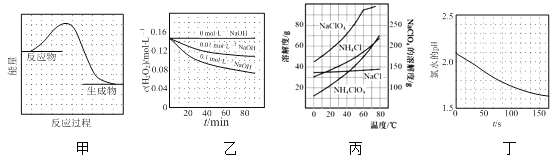
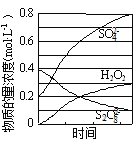
(2)“反应”中部分物质的浓度变化如图所示,该反应的离子方程式为______。
(3)双氧水中H2O2的含量可以用酸性KMnO4溶液来测定,测定时MnO![]() 被还原成Mn2+,测定反应的离子方程式为______。
被还原成Mn2+,测定反应的离子方程式为______。
(4)pH=6时,(NH4)2S2O8溶液与足量MnSO4反应有MnO2沉淀生成,过滤后所得滤液中含硫微粒均为SO42-,该反应的离子方程式为______。
【答案】2NH4HSO4![]() (NH4)2S2O8+H2↑ S2O82-+2H2O=H2O2+2SO42-+2H+ 2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O S2O82-+Mn2++2H2O=MnO2↓+2SO42-+4H+
(NH4)2S2O8+H2↑ S2O82-+2H2O=H2O2+2SO42-+2H+ 2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O S2O82-+Mn2++2H2O=MnO2↓+2SO42-+4H+
【解析】
根据工艺流程和题中信息可看出,电解NH4HSO4可生成氢气和(NH4)2S2O8,(NH4)2S2O8在酸性条件下发生水解会生成H2O2和NH4HSO4,最后蒸馏得到H2O2,据此分析作答。

【题目】CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
已知反应Fe(s)+CO2(g)![]() FeO(s)+CO(g)的平衡常数为K1;
FeO(s)+CO(g)的平衡常数为K1;
反应Fe(s)+H2O(g)![]() FeO(s)+H2(g)的平衡常数为K2。
FeO(s)+H2(g)的平衡常数为K2。
在不同温度时K1、K2的值如下表:
温度(绝对温度) | K1 | K2 |
973 | 1.47 | 2.38 |
1173 | 2.15 | 1.67 |
(1)推导反应CO2(g)+H2(g)![]() CO(g)+H2O(g)的平衡常数K与K1、K2的关系式:_____________________。
CO(g)+H2O(g)的平衡常数K与K1、K2的关系式:_____________________。
(2)通过K值的计算,(1)中的反应是_________反应(填“吸热”或“放热”)。
(3)在一体积为10L的密闭容器中,加入一定量的CO2和H2O(g),在1173开时发生反应并记录前5min的浓度,第6min时改变了反应的条件。各物质的浓度变化如下表:
时间/min | CO2 | H2O | CO | H2 |
0 | 0.2000 | 0.3000 | 0 | 0 |
2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | |
5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
6 | 0.0350 | 0.1350 | 0.1650 |
①前2min,用CO表示的该化学反应的速率是:_______________________。
②在3~4min之间,反应处于___________状态(填“平衡”或“非平衡”)。
③第6min时,平衡向_________方向移动,可能的原因是______________________。