题目内容
CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-889.5kJ·mol-1
C2H6(g)+27O2(g)=2CO2(g)+3H2O(l)ΔH=-1583.4kJ·mol-1
C2H4(g)+3O2(g)=2CO2(g)+2H2O(l)ΔH=-1409.6kJ·mol-1
C2H2(g)+25O2(g)=2CO2(g)+H2O(l)ΔH=-1298.4kJ·mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)ΔH=-2217.8kJ·mol-1
如果1mol上述烃中的两种混合物完全燃烧后放出1518.8的热量,则下列组合不可能是( )
C2H6(g)+27O2(g)=2CO2(g)+3H2O(l)ΔH=-1583.4kJ·mol-1
C2H4(g)+3O2(g)=2CO2(g)+2H2O(l)ΔH=-1409.6kJ·mol-1
C2H2(g)+25O2(g)=2CO2(g)+H2O(l)ΔH=-1298.4kJ·mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)ΔH=-2217.8kJ·mol-1
如果1mol上述烃中的两种混合物完全燃烧后放出1518.8的热量,则下列组合不可能是( )
| A.CH4和C2H4 | B.CH4和C2H6 |
| C.C3H8和C2H6 | D.C3H8和C2H2 |
AC
混合烃的平均燃烧热为1518.8kJ,则混合烃之一的燃烧热必大于1518.8kJ,另一烃燃烧热必小于1518.8kJ,代入各选项进行比较,可知正确的选项为A、C。

练习册系列答案
相关题目
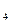 )的炉具,改成燃烧液化石油气(主要成分是C
)的炉具,改成燃烧液化石油气(主要成分是C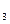 H
H 等)的炉具,其改造办法是( )
等)的炉具,其改造办法是( )