题目内容
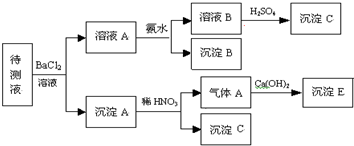
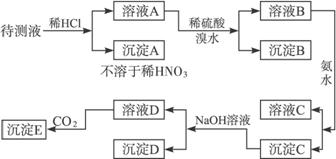
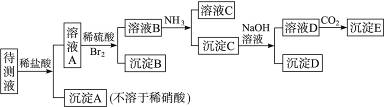
某待测溶液中可能含有Fe2+、Fe3+、Al3+、Ag+、Ba2+、NH![]() 、Ca2+等,进行 以下实验(所加酸、碱、氨水、溴水都是过量的)。
、Ca2+等,进行 以下实验(所加酸、碱、氨水、溴水都是过量的)。
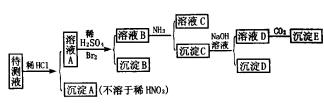
根据实验结果:
(1)判断待测液中有无Ba2+、Ca2+,并写出理由。
(2)写出沉淀D的化学式。
(3)写出从溶液D生成沉淀E的离子反应方程式。
答案:
解析:
解析:
(1)至少有其中的一种,因BaSO4不溶于水、CaSO4微溶于水(2)Fe(OH)3(3)AlO
|

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目