题目内容
【题目】过碳酸钠(2Na2CO3·3H2O2)广泛用于洗涤、纺织、医疗、造纸等。某兴趣小组展开了深入的学习:
【资料卡片】:

I、制备研究:工业上采用“醇析法”将其转化成固态的过碳酸钠晶体(化学式为2Na2CO3·3H2O2), “醇析法”的生产工艺流程如下:
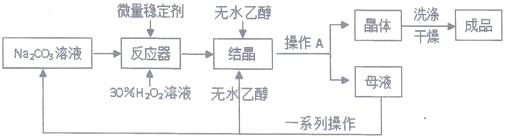
请回答问题:
(1)Na2CO3俗名:_______________;其水溶液能使酚酞变_______________;
(2)H2O2受热容易分解,写出该分解反应的方程式:_________________;
(3)生产过程中,反应及干燥均需在低温度下进行,原因是________________;
(4)生产过程中,加入较多无水乙醇后,过碳酸钠晶体大量析出,此无水乙醇的作用可能是_________________;
(5)操作A的名称是______________,若在实验室完成此操作,需要的玻璃仪器是烧杯、玻璃棒和_____________;
(6)母液可以循环使用,但须进行“一系列操作”分离,这些操作包括:加入少量___________,不再有气泡产生后,过滤,将所得滤液再进行______________(填操作名称),即可得Na2CO3溶液和95%的乙醇。为获取无水乙醇,还需进行的操作是:向95%的乙醇中加入足量CaO后,选__________(填序号)装置进行实验。
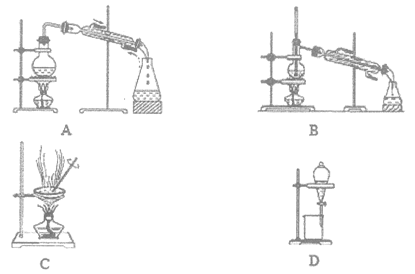
II、纯度测定:兴趣小组同学设计了如图1所示实验装置(部分仪器略去),测定过碳酸钠样品中2Na2CO3·3H2O2的质量分数。步骤如下:
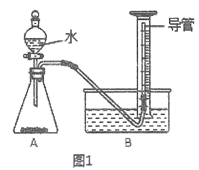
① 连接仪器并检查好气密性
② 将过碳酸钠样品(2.20g)和少许MnO2均匀混合后置于装置A中,在量筒中加满水;
③ 连接仪器,打开滴液漏斗活塞,缓缓滴入水;
④ 待装置A中_____________时,停止滴加水,并关闭活塞;
⑤ 冷却至室温后,平视读数;
⑥ 根据数据进行计算。
请回答下列问题:
(7)完善实验步骤的相关内容:④ __________;
(8)第⑤中,已“冷却至室温”的判断依据是:_____________;
(9)量筒中,加装的长导管的作用是:______________;
(10)实验中,______________,则开始收集气体;
A.刚开始出现气泡时
B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
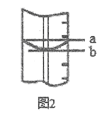
(11)量筒的局部示意见图2,平视读数时应沿____________视线(选填“a”或“b”) 进行。图中________视线(选填“a”或“b”)对应的读数较大。
(12)若量筒中收集到气体的体积是224mL (己转化为标准状况下的数据),计算过碳酸钠样品中2Na2CO3·3H2O2的质量分数:_____________;[Mr(O2)=32、Mr(2Na2CO3·3H2O2)=314]
(13)经过讨论,小组同学一致认为测定结果偏大,理由是_________________(任写一种)。
【答案】
I、(1)纯碱;红;
(2)2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)H2O2和2Na2CO3·3H2O2受热都容易分解;
(4)无水乙醇能降低过碳酸钠溶解度;
(5)过滤;漏斗;
(6)MnO2;蒸馏;A;
II、(7)无气泡冒出(或无明显现象);
(8)量筒内液面不再变化;
(9)防止冷却时,(短导管)将量筒中的水倒吸入A中影响测量;
(10)A;
(11)b;b;
(12)95%或95.1%;
(13)①滴液漏斗中的水进入A中,挤出一部分气体入量筒中
②量筒中导气管占有部分空间
③当量筒中的液面高于水槽中的时,量筒内部气压小于外界大气压,使测量的气体体积偏大。
【解析】
试题分析:I、(1)Na2CO3俗名是纯碱;其水溶液水解显碱性,能使酚酞变红色,故答案为:纯碱;红;
(2)H2O2受热容易分解,分解反应的方程式为2H2O2![]() 2H2O+O2↑,故答案为:2H2O2
2H2O+O2↑,故答案为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)过氧化氢和过碳酸钠在加热时均会分解,因此生产过程中,反应及干燥均需在低温度下进行,故答案为:H2O2和2Na2CO3·3H2O2受热都容易分解;
(4)生产过程中,加入较多无水乙醇后,无水乙醇能降低过碳酸钠溶解度,使得过碳酸钠晶体大量析出,故答案为:无水乙醇能降低过碳酸钠溶解度;
(5)分离出过碳酸钠晶体,可以用过滤的方法进行,过滤存在需要的玻璃仪器有烧杯、玻璃棒和漏斗,故答案为:过滤;漏斗;
(6)母液中是饱和过碳酸钠溶液,其中的过碳酸钠可以循环使用,要得到Na2CO3溶液和95%的乙醇,需要首先使过氧化氢分解,可以加入二氧化锰作催化剂,分离Na2CO3溶液和乙醇,可以利用乙醇易挥发的性质选用蒸馏进行分离,为获取无水乙醇,还需进行的操作是:向95%的乙醇中加入足量CaO后蒸馏,故选装置A,故答案为:MnO2;蒸馏;A;
II、(7)根据实验操作过程,④待装置A中不再产生气泡时,停止加水,并关闭活塞,故答案为:无气泡冒出;
(8)第⑤中,当量筒内液面不再变化,表明已“冷却至室温” ,故答案为:量筒内液面不再变化;
(9)量筒中,加装的长导管可以防止冷却时,(短导管)将量筒中的水倒吸入A中影响测量,故答案为:防止冷却时,(短导管)将量筒中的水倒吸入A中影响测量;
(10)开始锥形瓶中有空气,最后锥形瓶中留有制取的氧气,两者体积相同,所以一开始就应当收集,故选A;
(11)量筒的局部示意见图2,平视读数时使溶液的凹液面与刻度相切,故选b;量筒的刻度是从下向上标注的,该量筒倒置,因此图中b对应的读数较大,故答案为:b;b;
(12)过碳酸钠分解产生氧气质量为224mL×10-3×1.43gL-1=0.32g
2(2Na2CO33H2O2)~3O2↑
628 96
x 0.32g
![]() =
=![]() ,解得:x=2.09g,则样品中,2Na2CO33H2O2的质量分数为:
,解得:x=2.09g,则样品中,2Na2CO33H2O2的质量分数为:![]() ×100%=95.0%,故答案为:95%;
×100%=95.0%,故答案为:95%;
(13)滴入的水占据了锥形瓶内的体积,或者量筒中导气管占有部分空间,或者当量筒中的液面高于水槽中的时,量筒内部气压小于外界大气压,都会使测量的气体体积偏大,导致测定结果偏大,故答案为:滴入的水占据了锥形瓶内的体积,使得O2体积偏大(或者量筒中导气管占有部分空间、当量筒中的液面高于水槽中的时,量筒内部气压小于外界大气压,)

 优学名师名题系列答案
优学名师名题系列答案

