题目内容
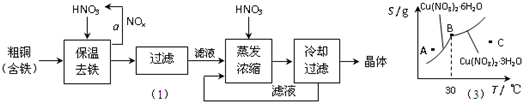
(2009?东城区二模)某化学课外活动小组设计实验探究氮的化合物的性质,装置如图所示(A装置未画出),其中A为气体发生装置.A中所用试剂从下列固体物质中选取:a.NH4HCO3、b.NH4Cl、c.Ca(OH)2、d.NaOH
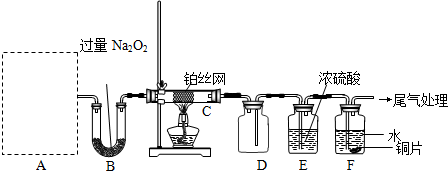
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯.部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:
(3)对于C中发生的可逆反应,下列说法正确的是
a.增大一种反应物的浓度可以提高另一种反应物的转化率
b.工业上进行该反应时,可采取高压的条件提高反应物转化率
c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
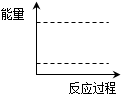
(4)请在下图坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式
 .
.
(5)待实验结束后,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是

检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯.部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
a
a
(填备选试剂的字母);此时A中主要的玻璃仪器有试管、酒精灯
试管、酒精灯
(填名称).(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:
2Na2O2+2H2O=4NaOH+O2 或2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2H2O=4NaOH+O2 或2Na2O2+2CO2=2Na2CO3+O2
.(3)对于C中发生的可逆反应,下列说法正确的是
a
a
.a.增大一种反应物的浓度可以提高另一种反应物的转化率
b.工业上进行该反应时,可采取高压的条件提高反应物转化率
c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
(4)请在下图坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式



(5)待实验结束后,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是
0.25
0.25
mol,甲在标准状况下是2.8
2.8
L(忽略气体的溶解).分析:(1)碳酸氢铵受热分解产生氨气、水和二氧化碳,固体加热分解可以在大试管中进行;
(2)二氧化碳和过氧化钠反应生成碳酸钠和氧气,水和过氧化钠反应生成氢氧化钠和氧气;
(3)先写出反应方程式,根据反应方程式判断正误;
(4)撤去C处酒精灯,铂丝继续保持红热,说明该反应是放热反应,根据能量守恒判断反应物和生成物的能量相对大小;
(5)先判断溶液中的溶质,根据钠原子守恒计算过氧化钠的物质的量;盐酸与碳酸钠反应生成的二氧化碳与碳酸氢铵分解生成的二氧化碳相同,根据反应方程式判断二氧化碳和水及过氧化钠之间的关系式,从而计算二氧化碳的体积.
(2)二氧化碳和过氧化钠反应生成碳酸钠和氧气,水和过氧化钠反应生成氢氧化钠和氧气;
(3)先写出反应方程式,根据反应方程式判断正误;
(4)撤去C处酒精灯,铂丝继续保持红热,说明该反应是放热反应,根据能量守恒判断反应物和生成物的能量相对大小;
(5)先判断溶液中的溶质,根据钠原子守恒计算过氧化钠的物质的量;盐酸与碳酸钠反应生成的二氧化碳与碳酸氢铵分解生成的二氧化碳相同,根据反应方程式判断二氧化碳和水及过氧化钠之间的关系式,从而计算二氧化碳的体积.
解答:解:(1)根据题意:C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯,铂丝继续保持红热,F处铜片逐渐溶解,说明有硝酸生成,所以A中获得的是氨气,加热NH4HCO3分解可以产生氨气,固体加热分解可以在大试管中进行,故答案为:a;试管、酒精灯;
(2)二氧化碳和过氧化钠反应生成碳酸钠和氧气,水和过氧化钠反应生成氢氧化钠和氧气,故答案为:2Na2O2+2H2O=4NaOH+O2 或2Na2O2+2CO2=2Na2CO3+O2;
(3)氨气和氧气在催化剂条件下能反应生成一氧化氮和水,4NH3 十 5O2
4NO+6H2O,
a.增大一种反应物的浓度,使反应向正反应方向移动,所以可以提高另一种反应物的转化率,故正确;
b.工业上进行该反应时,采取高压的条件反应向逆反应方向移动,所以反应物转化率降低,故错误;
c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比可能是4:5,这与反应物的初始浓度和转化率有关,故错误;
故选a.
(4)撤去C处酒精灯,铂丝继续保持红热,说明该反应是放热反应,根据能量守恒知,反应物的能量大于生成物的能量,
 ,故答案为:
,故答案为: ;
;
(5)水和过氧化钠反应生成氢氧化钠和氧气,二氧化碳和过氧化钠反应生成碳酸钠和氧气,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,所以溶液中的溶质是氯化钠,根据钠原子守恒计算过氧化钠的物质的量,HCl--NaCl--
Na2O2
1
1mol?L-1×0.5L 0.25mol
所以过氧化钠的物质的量为0.25mol.
NH4HCO3
NH3↑+H2O+CO2↑
2H2O+2Na2O2=4NaOH+O2↑
2CO2+2Na2O2=2Na2CO3+O2
根据方程式知,碳酸氢铵分解生成的水和二氧化碳的物质的量相同,水和二氧化碳分别与过氧化钠反应需要的过氧化钠的物质的量相同,都是0.125mol;
碳酸氢铵生成的二氧化碳和过氧化钠反应生成碳酸钠,碳酸钠和盐酸反应生成的二氧化碳,所以碳酸钠与盐酸反应生成的二氧化碳和碳酸氢铵分解生成的二氧化碳相同.
设二氧化碳的体积为V.
2CO2+2Na2O2=2Na2CO3+O2
44.8L 2mol
V 0.125mol
V=2.8L
故答案为:0.25;2.8.
(2)二氧化碳和过氧化钠反应生成碳酸钠和氧气,水和过氧化钠反应生成氢氧化钠和氧气,故答案为:2Na2O2+2H2O=4NaOH+O2 或2Na2O2+2CO2=2Na2CO3+O2;
(3)氨气和氧气在催化剂条件下能反应生成一氧化氮和水,4NH3 十 5O2
| Pt |
| △ |
a.增大一种反应物的浓度,使反应向正反应方向移动,所以可以提高另一种反应物的转化率,故正确;
b.工业上进行该反应时,采取高压的条件反应向逆反应方向移动,所以反应物转化率降低,故错误;
c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比可能是4:5,这与反应物的初始浓度和转化率有关,故错误;
故选a.
(4)撤去C处酒精灯,铂丝继续保持红热,说明该反应是放热反应,根据能量守恒知,反应物的能量大于生成物的能量,
 ,故答案为:
,故答案为: ;
;(5)水和过氧化钠反应生成氢氧化钠和氧气,二氧化碳和过氧化钠反应生成碳酸钠和氧气,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,所以溶液中的溶质是氯化钠,根据钠原子守恒计算过氧化钠的物质的量,HCl--NaCl--
| 1 |
| 2 |
1
| 1 |
| 2 |
1mol?L-1×0.5L 0.25mol
所以过氧化钠的物质的量为0.25mol.
NH4HCO3
| ||
2H2O+2Na2O2=4NaOH+O2↑
2CO2+2Na2O2=2Na2CO3+O2
根据方程式知,碳酸氢铵分解生成的水和二氧化碳的物质的量相同,水和二氧化碳分别与过氧化钠反应需要的过氧化钠的物质的量相同,都是0.125mol;
碳酸氢铵生成的二氧化碳和过氧化钠反应生成碳酸钠,碳酸钠和盐酸反应生成的二氧化碳,所以碳酸钠与盐酸反应生成的二氧化碳和碳酸氢铵分解生成的二氧化碳相同.
设二氧化碳的体积为V.
2CO2+2Na2O2=2Na2CO3+O2
44.8L 2mol
V 0.125mol
V=2.8L
故答案为:0.25;2.8.
点评:本题考查了氨气的制取和性质,难度较大,易错题是(5),会分析整个装置反应过程是解本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
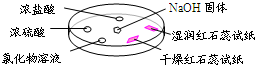 (2009?东城区二模)如图,利用培养皿探究氨气的性质.实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面.下表中对实验现象所做的解释正确的是( )
(2009?东城区二模)如图,利用培养皿探究氨气的性质.实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面.下表中对实验现象所做的解释正确的是( )
 NH4++NH2-,由此制备无水硝酸铜的方法之一是用Cu与液态N2O4反应.液态N2O4电离得到的两种离子所含电子数相差18,则液态N2O4电离的方程式是
NH4++NH2-,由此制备无水硝酸铜的方法之一是用Cu与液态N2O4反应.液态N2O4电离得到的两种离子所含电子数相差18,则液态N2O4电离的方程式是