题目内容
【题目】下列图示与对应的叙述相符的是( )
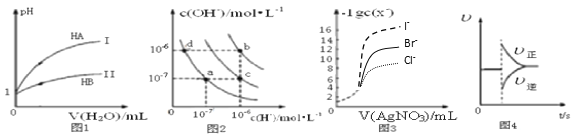
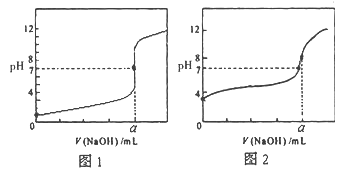
A. 图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则等物质的量浓度的NaA和NaB混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+)
B. 图2中在b点对应温度下,将pH=2的H2SO4溶液与pH=12的NaOH溶液等体积混合后,溶液显中性
C. 用0.0100 mol/L硝酸银标准溶液,滴定浓度均为0.1000 mol/L Cl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl-
D. 图4表示在N2(g)+3H2(g) ![]() 2NH3(g)达到平衡后,减小NH3浓度时速率的变化
2NH3(g)达到平衡后,减小NH3浓度时速率的变化
【答案】A
【解析】
A、根据图1,相同pH时,稀释相同倍数,酸性强的pH变化大,即HA的酸性强于HB,依据越弱越水解的规律,A-水解程度弱于B-,离子浓度大小顺序是c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+),故A正确;
B、b点对应温度下,水的离子积为10-12,H2SO4中c(H+)=10-2mol·L-1,NaOH溶液中c(OH-)=1mol·L-1,等体积混合后,NaOH过量,溶液显碱性,故B错误;
C、根据图像,纵坐标是-lgc(X-),数值越大,c(X-)越小,在c(Ag+)相同时,c(X-)越小,Ksp(AgX)越小,即I-先沉淀出来,故C错误;
D、根据图像,改变条件瞬间,v正增大,v逆减小,可能是增大反应物浓度,同时减少生成物浓度,如果只减少NH3的浓度,只降低v逆,v正不变,故D错误。

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目