题目内容
1.某校化学兴趣小组为探究铁与浓硫酸反应,设计了图1、图2所示装置进行实验.
(1)比较两实验装置,图2装置的优点是:①能更好的吸收有毒气体SO2,防止其污染环境; ②便于控制反应的发生和停止.
(2)导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到“液封”作用阻止SO2气体逸出而防止污染环境;二是停止加热时,能防止倒吸或平衡压强.
(3)能说明有SO2气体产生的实验现象是品红溶液褪色.C中发生反应的离子方程式:SO2+2OH-=SO32-+H2O
(4)反应一段时间后,用滴管吸取A试管中的溶液滴入适量水中为试样,试样中所含金属离子的成分有以下三种可能:
Ⅰ:只含有Fe3+;Ⅱ:只含有Fe2+;Ⅲ:既有Fe3+又有Fe2+.
为验证Ⅱ、Ⅲ的可能性,选用如下试剂,填写下列空格:
A.稀HCl溶液 B.稀H2SO4硫酸 C.KSCN溶液 D.KMnO4溶液
E.NaOH溶液 F.淀粉KI溶液 G.H2O2溶液
验证Ⅱ:取试样,先滴加少量的C(填试剂序号,下同),振荡,再滴加少量的G,根据溶液颜色的变化可确定假设Ⅱ是否正确.
验证Ⅲ:步骤1.取试样,滴加少量的C(或F)(填试剂序号),溶液的颜色变红(或蓝)色.则试样中含有Fe3+,发生反应的离子方程式为Fe3++3SCN-═Fe(SCN)3或2I-+2Fe3+=I2+2Fe2+.
步骤2.再取适量的试样滴加到少量的D(填试剂序号),溶液的颜色变为紫红色褪去或变浅、色,则试样中含有Fe2+,此反应的离子方程式为:5Fe2++MO4-+8H+=5Fe3++Mn2++4H2O.
分析 (1)图2装置中Fe丝可以抽动,能控制反应的发生和停止,有尾气处理装置;
(2)导气管e与外界连通能起到平衡压强防止倒吸的作用;
(3)二氧化硫能够使品红溶液褪色;二氧化硫为酸性氧化物,与氢氧化钠溶液反应生成亚硫酸钠和水;
(4)验证Ⅱ:检验Fe2+,先加KSCN溶液,再加H2O2溶液;
验证Ⅲ:步骤1.检验Fe3+,加KSCN溶液,变红色;或加淀粉KI溶液,变蓝色;
步骤2.既有Fe3+又有Fe2+时,检验Fe2+要加酸性KMnO4溶液.
解答 解:(1)图2装置中Fe丝可以抽动,能控制反应的发生和停止,而且有尾气处理装置,
故答案为:便于控制反应的发生和停止;
(2)导气管e与外界连通,停止加热时能起到平衡压强防止倒吸的作用,
故答案为:停止加热时,能防止倒吸或平衡压强;
(3)二氧化硫具有漂白性,能是品红溶液褪色,所以若品红溶液褪色,证明有二氧化硫气体产生;二氧化硫与氢氧化钠溶液反应的离子方程式为:SO2+2OH-=SO32-+H2O,
故答案为:品红溶液褪色;SO2+2OH-=SO32-+H2O;
(4)Ⅱ为只含有Fe2+,验证Ⅱ时,需要先加KSCN溶液,溶液不变红,然后再加H2O2溶液,若此时溶液变成红色,则证明只含有亚铁离子,
故答案为:C,G;
Ⅲ为既有Fe3+又有Fe2+;验证Ⅲ的方法为:步骤1:检验Fe3+,加KSCN溶液,变红色,发生的反应为:Fe3++3SCN-═Fe(SCN)3;或加淀粉KI溶液,变蓝色,其反应为:2I-+2Fe3+=I2+2Fe2+;
故答案为:C(或F);红(或蓝),Fe3++3SCN-═Fe(SCN)3或2I-+2Fe3+=I2+2Fe2+;
步骤2.再验证亚铁离子,需要使用酸性高锰酸钾溶液,方法为:加酸性KMnO4溶液,高锰酸钾溶液褪色证明有二价铁离子,反应的离子方程式为:5Fe2++MO4-+8H+=5Fe3++Mn2++4H2O,
故答案为:D;紫红色褪去或变浅;5Fe2++MO4-+8H+=5Fe3++Mn2++4H2O.
点评 本题通过浓硫酸的性质,侧重考查性质实验方案的设计与评价,题目难度中等,明确铁离子、亚铁离子的检验方法为解答关键,注意掌握性质实验方案的设计原则,试题充分考查了学生的分析能力及化学实验能力.

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案| 选项 | 实验操作 | 现象 | 结论 |
| A | 蘸有浓氨水的玻璃棒靠近某溶液 | 有白烟产生 | 该溶液可能是浓盐酸 |
| B | 将SO2通入Ba(NO3)2溶液 | 产生白色沉淀 | SO2与可溶性钡盐均可生成白色沉淀 |
| C | 将湿润淀粉碘化钾试纸检验某溶液 | 试纸变蓝 | 该溶液一定是氯水 |
| D | 用铂丝蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 该溶液一定是钠盐溶液 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 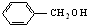 和 和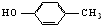 | B. | 乙酸和硬脂酸 | ||
| C. | 苯甲酸和  | D. | 硝基乙烷(CH3CH2NO2)和氨基乙酸5 |

| A. | 甲装置:用所示装置分离出溴苯 | |
| B. | 乙装置:加热浓硫酸和乙醇混合液,制取乙烯 | |
| C. | 丙装置:加热苯和硝基苯的混合物,分离出苯 | |
| D. | 丁装置:验证溴乙烷发生消去反应生成烯烃 |
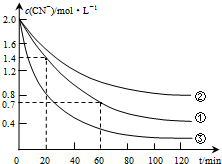 生产中可用双氧水氧化法处理电镀含氰废水,某化学兴趣小组模拟该法探究有关因素对破氰反应速率的影响(注:破氰反应是指氧化剂将CN-氧化的反应).
生产中可用双氧水氧化法处理电镀含氰废水,某化学兴趣小组模拟该法探究有关因素对破氰反应速率的影响(注:破氰反应是指氧化剂将CN-氧化的反应).【相关资料】
①氰化物主要是以CN-和[Fe(CN)6]3-两种形式存在.
②Cu2+可作为双氧水氧化法破氰处理过程中的催化剂;Cu2+在偏碱性条件下对双氧水分解影响较弱,可以忽略不计.
③[Fe(CN)6]3-较CN-难被双氧水氧化,且pH越大,[Fe(CN)6]3-越稳定,越难被氧化.
【实验过程】
在常温下,控制含氰废水样品中总氰的初始浓度和催化剂Cu2+的浓度相同,调节含氰废水样品不同的初始pH和一定浓度双氧水溶液的用量,设计如下对比实验:
(l) 请完成以下实验设计表(表中不要留空格)
| 实验 序号 | 实验目的 | 初始pH | 废水样品体积/mL | CuSO4溶液的体积/mL | 双氧水溶液的体积/mL | 蒸馏水的体积/mL |
| ① | 为以下实验操作参考 | 7 | 60 | 10 | 10 | 20 |
| ② | 废水的初始pH对破氰反应速率的影响 | 12 | 60 | 10 | 10 | 20 |
| ③ | 双氧水的浓度对破氰反应速率的影响 | 7 | 60 | 10 | 20 | 10 |
(2)实验①中20~60min时间段反应速率:υ(CN-)=0.0175mol•L-1•min-1.
(3)实验①和实验②结果表明,含氰废水的初始pH增大,破氰反应速率减小,其原因可能是初始pH增大,催化剂Cu2+会形成Cu(OH)2沉淀,影响了Cu2+的催化作用(或初始pH增大,[Fe(CN)6]3-较中性和酸性条件下更稳定,难以氧化)(填一点即可).在偏碱性条件下,含氰废水中的CN-最终被双氧水氧化为HCO3-,同时放出NH3,试写出该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-.
(4)该兴趣小组同学要探究Cu2+是否对双氧水氧化法破氰反应起催化作用,请你帮助他设计实验并验证上述结论,完成下表中内容.(己知:废水中的CN-浓度可用离子色谱仪测定)
| 实验步骤(不要写出具体操作过程) | 预期实验现象和结论 |
| A. | 苯的实验式 C6H6 | B. | 乙醇的分子式CH3CH2OH | ||
| C. | 乙烯的结构简式CH2CH2 | D. | 甲醛的结构式: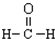 |
 某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图所示装置进行有关实验.
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图所示装置进行有关实验.
