题目内容
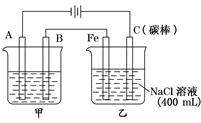
(20分)如图为相互串联的甲乙两个电解池,请回答:

(1)若甲池为电解精炼粗铜(含有锌铁镍银金和铂等微量杂质,杂质发生的电极反应不必写出)装置,电解液选用CuSO4溶液,则:
①A电极发生的反应类型为 ; B电极和Fe电极电子的流向由 到 (填B或Fe)。
②B电极的材料是____________,电极反应式为___________ _______。
CuSO4溶液的浓度 (填 “不变”“略有增加”或“略有减少”)
(2)实验开始时,若在乙池两边电极附近同时各滴入几滴酚酞试液,则:
①写出电解NaCl溶液总的化学方程式
。
②在Fe极附近观察到的现象是____ ________。检验碳棒电极反应产物的方法是 _。
(3)若甲槽电解液为CuSO4,实验中发现阴极增重12.8g,则乙槽阴极放出气体在标准状况下的体积为_____ ____L。若乙槽剩余液体为400mL,则电解后得到碱液的物质的量浓度为_______ ___ 。
(1) ① 还原反应 B到Fe(共2分)
② 粗铜 Cu - 2e - = Cu2+ 略有减少
(2) ①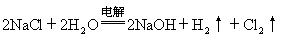 ,②溶液变红。 把湿润的碘化钾淀粉试纸放在碳棒附近,试纸变蓝色。(3)4.48L (4)1mol·L-1
,②溶液变红。 把湿润的碘化钾淀粉试纸放在碳棒附近,试纸变蓝色。(3)4.48L (4)1mol·L-1
【解析】(1)根据装置图可看出,A是阴极、B是阳极、铁是阴极、碳棒是阳极。所以A电极发生还原反应,B发生氧化反应,电子由B电极通过导线传递到铁电极上。粗铜精炼时阳极必须连粗铜,电极反应式为Cu - 2e - = Cu2+。由于粗铜中含有比铜活泼的金属,当这些活泼的金属失电子时,在阴极上溶液的铜离子放电,所以CuSO4溶液的浓度略有减少。
(2)乙池是电解NaCl溶液的,阳极是碳棒,溶液中的氯离子放电,生成氯气,检验氯气可利用其氧化性通过湿润的碘化钾淀粉试纸来检验。铁是阴极,溶液中由水电离出来的氢离子生成氢气,所以在阴极周围溶液显碱性。
(3)阴极增重12.8g,说明析出铜是0.2mol,转移电子0.4mol。根据得失电子守恒可知乙槽阴极放出氢气是0.2mol,在标准状况下的体积为4.48L。根据电解的总方程式可知生成氢氧化钠是0.4mol,电解后得到碱液的物质的量浓度为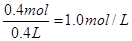
。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案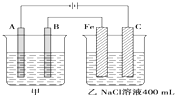 如图为相互串联的甲乙两个电解池,请回答:
如图为相互串联的甲乙两个电解池,请回答: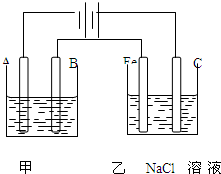 如图为相互串联的甲乙两个电解池,请回答:
如图为相互串联的甲乙两个电解池,请回答: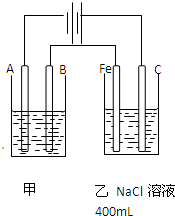 如图为相互串联的甲乙两个电解池,请回答:
如图为相互串联的甲乙两个电解池,请回答: