题目内容
2.以下说法正确的是( )| A. | 金属钠着火时可以用泡沫灭火器灭火 | |
| B. | 氯气可用于自来水的消毒 | |
| C. | 钠比铜活泼,因而钠可以从CuCl2溶液中置换出铜 | |
| D. | 氢氧化钠常用于治疗胃酸过多 |
分析 A.金属钠燃烧生成的过氧化钠可以和二氧化碳之间反应,泡沫灭火器产生的是二氧化碳;
B.氯气和水反应生成次氯酸具有氧化性漂白性;
C.钠可以与CuCl2溶液反应,但先发生Na与水的反应;
D.氢氧化钠碱性太强,腐蚀性太强.
解答 解:A.钠和水反应生成氢气,氢气是易燃物,钠燃烧后生成过氧化钠,过氧化钠和水、二氧化碳反应生成氧气,促进钠的燃烧,所以钠着火燃烧时,不能用泡沫灭火器灭火,应该用沙子灭火,故A错误;
B.氯气和水反应生成次氯酸具有氧化性漂白性;氯气可用于自来水消毒,故B正确;
C.钠可以与CuCl2溶液反应,先发生Na与水的反应,生成的碱再与盐溶液反应,不会置换出金属Cu,故C错误;
D.氢氧化钠碱性太强,腐蚀性太强,所以不能用于治疗胃酸过多,故D错误;
故选:B.
点评 本题考查化学实验基本操作,题目难度不大,注意根据物质的性质进行判断,学习中注重相关知识的积累.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
9.下列实验现象与结论不一致的是
( )
| 实验操作(或设计) | 实验现象 | 结论 | |
| A | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | HA放出的氢气多且反应速率快 | 酸性:HB>HA |
| B | 以镁、铝、氢氧化钠溶液构成原电池 | 镁表面有气泡 | 镁作原电池的负极 |
| C | 相同温度下,等质量的大理石与等体积等浓度的盐酸反应 | 粉状大理石产生气泡更快 | 反应速率: 粉状大理石>块状大理石 |
| D | 向盛有10滴0.1mol•L-1 AgNO3溶液的试管中滴加0.1mol•L-1 NaCl溶液,至不再有沉淀生成,再向其中滴加0.1mol•L-1 NaI溶液 | 先有白色沉淀,后转成黄色沉淀 | Ksp(AgCl )>Ksp (AgI) |
| A. | A | B. | B | C. | C | D. | D |
13. 一定温度下在2L容器内进行某一反应,气体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在2L容器内进行某一反应,气体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
 一定温度下在2L容器内进行某一反应,气体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在2L容器内进行某一反应,气体X、气体Y的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )| A. | 反应的化学方程式为4X?Y | |
| B. | t2时,正反应速率等于逆反应速率 | |
| C. | t3时,Y浓度不再变化,反应达到平衡 | |
| D. | 当t1=2时,用X表示该反应在2 min内的平均反应速率为0.25mol/(L•min) |
10.下列物质中不属于天然高分子化合物的是( )
| A. | 纤维素 | B. | 淀粉 | C. | 蛋白质 | D. | 麦芽糖 |
17.如图为某化学反应的能量-反应进程图,由此可判断该反应( )
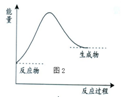

| A. | 为放热反应 | B. | 为吸热反应 | C. | 属于燃烧反应 | D. | 属于中和反应 |
7.下列物质中,能使酸性高锰酸钾溶液褪色的是( )
| A. | CH4 | B. | CH2=CH2 | C. | CH3CH3 |
14.向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得到深蓝色透明溶液.若加入乙醇将析出深蓝色晶体.下列说法正确的是( )
| A. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 | |
| B. | 在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤对电子 | |
| C. | 沉淀溶解后将生成深蓝色的正四面体形的配离子[Cu(NH3)4]2+ | |
| D. | 加入极性较小的溶剂乙醇后,将析出[Cu(H2O)4]SO4•H2O晶体 |
11.下列关于化学键和分子间作用力的说法中不正确的是( )
| A. | 化学键是一种作用力 | |
| B. | 化学键可以使离子相结合,也可以使原子相结合 | |
| C. | 一种物质只含两种非金属元素,该物质中一定没有非极性供价键 | |
| D. | 氢键属于分子间作用力,不属于化学键 |
12.当下列物质以晶体形式存在时,其所属晶体类型和所含化学键类型分别相同的是( )
| A. | 氯化钠、氯化氢 | B. | 二氧化碳、二氧化硅 | ||
| C. | 四氯化碳、四氯化硅 | D. | 单质铁、单质碘 |