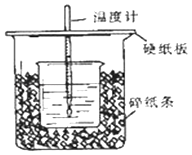
题目内容
【题目】下列图示中,A是一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应的火焰均呈黄色。
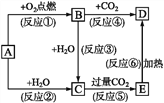
填写下列空白:
(1)写出化学式:A_____,B_____,D______________。
(2)以上反应中属于氧化还原反应的有_____(填序号)。
(3)写出反应⑤的离子方程式:___。写出反应⑥的化学方程式:___。
【答案】 Na Na2O2 Na2CO3 ①②③④ OH-+CO2![]() HCO3- 2NaHCO3
HCO3- 2NaHCO3![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
【解析】本题考查无机推断,这些物质的焰色反应为黄色,说明含有Na元素,A为单质,B、C、D、E是含A元素的常见化合物,则A为Na,反应①为2Na+O2![]() Na2O2,即B为Na2O2,反应②发生2Na+2H2O=2NaOH+H2↑,即C为NaOH,反应③为2Na2O2+2H2O=4NaOH+O2↑,反应④发生2Na2O2+2CO2=2Na2CO3+O2,即D为Na2CO3,反应⑤是NaOH与过量CO2反应,即反应方程式为NaOH+CO2=NaHCO3,即E为2NaHCO3
Na2O2,即B为Na2O2,反应②发生2Na+2H2O=2NaOH+H2↑,即C为NaOH,反应③为2Na2O2+2H2O=4NaOH+O2↑,反应④发生2Na2O2+2CO2=2Na2CO3+O2,即D为Na2CO3,反应⑤是NaOH与过量CO2反应,即反应方程式为NaOH+CO2=NaHCO3,即E为2NaHCO3![]() Na2CO3+CO2↑+H2O,(1)根据上述分析,A为Na,B为Na2O2,D为Na2CO3;(2)上述发生氧化还原反应的有①②③④;(3)反应⑤的离子反应方程式为OH-+CO2=HCO3-,反应⑥的化学反应方程式为:2NaHCO3
Na2CO3+CO2↑+H2O,(1)根据上述分析,A为Na,B为Na2O2,D为Na2CO3;(2)上述发生氧化还原反应的有①②③④;(3)反应⑤的离子反应方程式为OH-+CO2=HCO3-,反应⑥的化学反应方程式为:2NaHCO3![]() Na2CO3+CO2↑+H2O。
Na2CO3+CO2↑+H2O。

【题目】某化学兴趣小组为探究浓硫酸的性质,设计了如下图所示的装置进行实验。
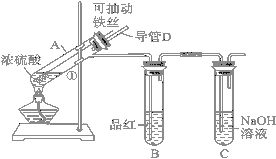
(1)用“可抽动的铁丝”代替“直接投入铁片”的优点是________________。
(2)说明SO2气体产生的实验现象是___________;装置C的作用是______________。
(3)反应一段时间后,他们对试管A中溶液的金属离子进行探究,请完成相关试题:
① 提出假设: 假设1:只含有Fe3+;
假设2:只含有Fe2+;
假设3:既有Fe2+,又有Fe3+。
② 请设计实验方案验证假设3。
限选试剂:稀硫酸、KMnO4溶液、KSCN溶液、NaOH溶液、H2O2溶液。
实验步骤 | 预期现象 |
步骤一:用胶头滴管取出A试管中的溶液,用水稀释后,并分装在试管Ⅰ、Ⅱ中备用 |
|
步骤二:检验Fe3+,往试管Ⅰ中,_____________ | _________________________ |
步骤三:检验Fe2+,往试管Ⅱ中,______________ | _________________________ |
(4)已知C+2H2SO4(浓)![]() 2SO2↑+CO2↑+2H2O,该反应体现浓硫酸的_____
2SO2↑+CO2↑+2H2O,该反应体现浓硫酸的_____
A.脱水性 B.强氧化性 C.吸水性
若要验证反应产物中同时混有SO2气体和CO2气体,可选择以下试剂进行实验:
NaOH溶液 ②品红溶液 ③溴水 ④Ca(OH)2溶液
选择合适试剂,并安排合理的顺序为_____________________(填序号)。