题目内容
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42﹣可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( ) 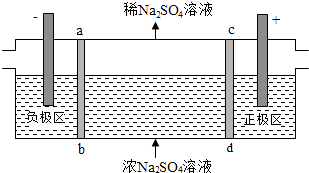
A.通电后中间隔室的SO42﹣离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极反应为2H2O﹣4e﹣=O2+4H+ , 负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成
【答案】B
【解析】解:A、阴离子向阳极(即正极区)移动,氢氧根离子放电pH减小,故A错误; B、直流电场的作用下,两膜中间的Na+和SO42﹣可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室,通电时,氢氧根离子在阳极区放电生成水和氧气,考虑电荷守恒,两膜中间的硫酸根离子会进入正极区,与氢离子结合成硫酸;氢离子在阴极得电子生成氢气,考虑电荷守恒,两膜中间的钠离子会进入负极区,与氢氧根离子结合成氢氧化钠,故可以得到NaOH和H2SO4产品,故B正确;
C、负极即为阴极,发生还原反应,氢离子得电子生成氢气,故C错误;
D、每生成1mol氧气转移4mol电子,当电路中通过1mol电子的电量时,会有0.25mol的O2生成,故D错误.
故选B.
A、阴离子向阳极(即正极区)移动,氢氧根离子放电pH减小;
B、从两极的电极反应和溶液的电中性角度考虑;
C、负极即为阴极,发生还原反应,氢离子放电;
D、当电路中通过1mol电子的电量时,会有0.25mol的O2生成.

练习册系列答案
相关题目