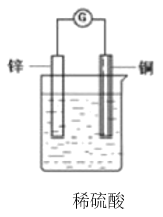
题目内容
【题目】H2A为二元弱酸。20℃时,配制一组c(H2A)+c(HA﹣)+c(A2﹣)=0.100molL﹣1的H2A和NaOH的混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如下图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
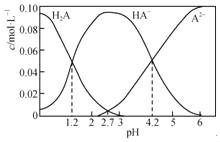
A. H2A的Ka1=10﹣1.2
B. pH=4.2的溶液中:c(HA﹣)=c(A2﹣)=0.050 molL﹣1
C. pH=7的溶液中:c(Na+)>2c(A2﹣)+c(H+)
D. c(Na+)=0.150 molL﹣1的溶液中:2c(OH﹣)+c(HA﹣)+3c(H2A)=2c(H+)+c(A2﹣)
【答案】AC
【解析】
A. 根据H2A的第一步电离平衡常数Ka1 = ![]() 作答;
作答;
B. 溶液中存在微弱的电离与水解,c(H2A) ![]() 0;
0;
C. 结合H2A的第二步电离平衡常数Ka2及电荷守恒规律分析作答;
D. 根据电荷守恒与物料守恒作答。
A. 从图中可看出,当pH = 1.2时,c(H2A) = c(HA-),则H2A的Ka1=![]() = 10-pH = 10-1.2,故A项正确;
= 10-pH = 10-1.2,故A项正确;
B. 从图中可看出,在pH=4.2的溶液中:c(HA-)=c(A2-),因有少许H2A图中未显示,结合题设条件c(H2A)+c(HA-)+c(A2-)=0.100 mol·L-1,则c(HA-)等于c(A2-)略小于0.050 mol/L,故B项错误;
C.其中在pH=4.2时,可计算出二元弱酸H2A的第二步电离平衡常数 = ![]() = 10-4.2在pH=7的溶液c(A2-)接近0.1 mol/L,c(H+)=10-7 mol/L,带入上述平衡常数表达式可得c(HA-) = 10-3.8> c(H+),根据电荷守恒规律又知c(Na+)=2c(A2-)+c(HA-),则c(Na+)>2c(A2-)+c(H+),故C项正确;
= 10-4.2在pH=7的溶液c(A2-)接近0.1 mol/L,c(H+)=10-7 mol/L,带入上述平衡常数表达式可得c(HA-) = 10-3.8> c(H+),根据电荷守恒规律又知c(Na+)=2c(A2-)+c(HA-),则c(Na+)>2c(A2-)+c(H+),故C项正确;
D. c(Na+)=0.150 mol·L-1的溶液中存在c(H2A)+c(HA-)+c(A2-)=0.100molL-1,则溶液中存在物料守恒2c(Na+)=3[c(H2A)+c(HA-)+c(A2-)]①,又存在电荷守恒c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)②,①-2×①得,2c(OH-)+c(A2-) =c(HA-)+3c(H2A) 2c(H+),故D项错误;
答案选AC。

 53随堂测系列答案
53随堂测系列答案【题目】综合题
Ⅰ.现有失去标签的CaCl2、AgNO3、HCl和Na2CO3四瓶溶液。为了确定这四瓶溶液成分,将四瓶溶液成分别编号为A、B、C、D后进行化学实验,实验记录如下:
实验顺序 | 实验内容 | 实验现象 |
① | A+B | 无现象 |
② | B+D | 有气体放出 |
③ | C+B | 有沉淀生成 |
④ | A+D | 有沉淀生成 |
请根据上述实验填空:
(1)A、C两瓶溶液分别是(用化学式表示)_____、______。
(2)A、D溶液混合恰好完全反应生成白色沉淀,过滤、洗涤,再向滤渣中加入足量盐酸溶液,写出向滤渣中加人盐酸的离子方程式: ______。
Ⅱ.某固体混合物中,可能含有下列离子中的几种:K+、NH4+、Mg2+、Ba2+、Cl-、SO42-、CO32-,将该混合物溶于水后得到澄清溶液,现取三份各100mL该溶液分别进行如下实验(已知:NH4++OH-NH3↑+H2O)。
(1)在一份溶液中加入AgNO3溶液,有白色沉淀生成。
(2)在另一份溶液中加入足量的NaOH 溶液并加热,收集到1.12L气体(标准状况下)。
(3)在第三份溶液中加入足量的BaCl2溶液后有沉淀生成,经称量其质量为6.27g,在该沉淀中加入足量的盐酸,沉淀部分溶解,剩余固体质量为2.33g。根据上述实验回答下列问题:
①溶液中一定不存在的离子是_______。
②溶液中一定存在的阴离子有______,其物质的量浓度分别为______ 。
③推断 K+是否存在并说理由:______。
【题目】氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。

请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。
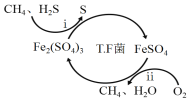
(1)过程i的离子反应方程式为_________________________________________。
(2)已知:
①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
pH | 0.7 | 1.1 | 1.5 | 1.9 | 2.3 | 2.7 |
Fe2+的氧化速率/g·L-1·h-1 | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 |
在转化脱硫中,请在上表中选择最佳pH范围是_______<pH<_______,这样选择的原因是:_______________________________________________。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。
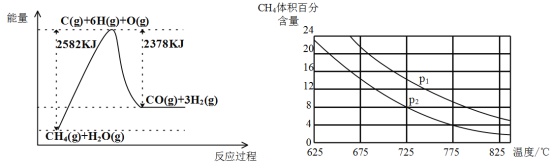
(3)①该过程的热化学方程式是__________________________________________。
②比较压强P1和p2的大小关系:P1 _________ P2(选填“>”“<”或“=”)。
③在一定温度和一定压强下的体积可变的密闭容器中充入1molCH4和1mol的水蒸气充分反应达平衡后,测得起始时混合气的密度是平衡时混合气密度的1.4倍,若此时容器的体积为2L,则该反应的平衡常数为______________(结果保留2位有效数字)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.H2提纯:将CO2和H2分离得到H2的过程如示意图
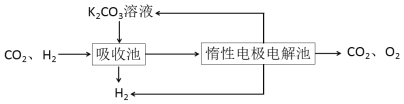
(4)吸收池中发生反应的离子方程式是____________________________________。