��Ŀ����
����Ŀ����2.0 L�����ܱ������г���1.0 mol PCl5�����¶�ΪT��ʱ�������·�ӦPCl5(g) ![]() PCl3(g)+C12(g) ��H��+124 kJ��mol��1����Ӧ�����вⶨ�IJ������ݼ��±���
PCl3(g)+C12(g) ��H��+124 kJ��mol��1����Ӧ�����вⶨ�IJ������ݼ��±���
ʱ��t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3��/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
�ش��������⣺
��1����Ӧ��ǰ50 s��ƽ������v(PCl5) ��______________��
��2���¶�ΪT��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ����________��
��3��Ҫ���������Ӧ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��________ (��дһ��) ��
��4�����¶�ΪT��ʱ������ʼʱ����0.5 mol PCl5��a mol Cl2��ƽ��ʱPCl5��ת������Ϊ20������a��________��
���𰸡�0.0016 mol/( L��s)0.025�����¶ȡ�����ѹǿ������PCl3��Cl2��0.1
��������
��1����Ӧ��ǰ50 s��ƽ������v(PCl3)=��c/��t=0.16mol��2.0L��50s=0.0016mol/(L��s)����������֮�Ⱥ�ϵ�������ȿ�֪��v(PCl5)= v(PCl3)= 0.0016mol/(L��s)���������������������0.0016 mol/( L��s)��
��2������v(PCl5)= v(PCl3)= 0.0016 mol/( L��s)���ɱ������ݿ��Կ��������¶�ΪT�棬����Ӧ�ﵽƽ��ʱ��n(PCl3)=0.2mol,n(C12)=0.2mol,n(PCl5)=0.8mol������c(PCl5)=0.4mol/L��c(PCl3)=0.1mol/L��c(C12)=0.1mol/L�����Ի�ѧƽ�ⳣ��K=c(PCl3)c(C12)/c(PCl5)= 0.1��0.1/0.4=0.025������������������ǣ�0.025��
��3�����ڸ÷�Ӧ������ӦΪ���������������ȷ�Ӧ������Ҫ���������Ӧ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�м�Сѹǿ���������¶Ȼ��ƽ�������з����PCl3��Cl2�ȴ�ʩ��������������������������¶ȡ�����ѹǿ������PCl3��Cl2�ȡ�
��4��������ʼʱ�������г���0.5molPCl5��amolCl2������ƽ��ʱPCl5��ת������Ϊ20������ﵽƽ��ʱn(PCl5)=0.4mol��n(PCl3)=0.1mol��n(Cl2)= (0.1+a)mol��c(PCl5)=0.2mol/L��c(PCl3)=0.05mol/L��c(Cl2)=(0.1+a)/2mol/L������ƽ�ⳣ��K=c(PCl3)c(C12)/c(PCl5)=0.025������������0.05��[(0.1+a)��2]/0.2=0.025�����a=0.1mol���������������������0.1��

����Ŀ��ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̡�
(1)��ˮ����ͨ�����ȵ�̿���ɲ���ˮú������ӦΪ��
C(s)��H2O(g)![]() CO(g)��H2(g) ��H����131.3 kJ��mol��1
CO(g)��H2(g) ��H����131.3 kJ��mol��1
��ʹ��ѧ��Ӧ���ʼӿ�Ĵ�ʩ��________(�����)��
������C�����ʵ��� �����߷�Ӧ�¶�
����ʱ����CO��H2ת��ΪCH3OH ���ܱն��������г���CO(g)
(2)����ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2 L�ĺ����ܱ������У����з�ӦCO(g)��H2O(g)CO2(g)��H2(g)���õ������������ݣ�
ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
2 | 900 | 2 | 4 | 0.8 | 3.2 | 3 |
��ʵ��1����v(CO2)��ʾ�Ļ�ѧ��Ӧ����Ϊ________��
�ڸ÷�Ӧ���淴ӦΪ________(������š�)�ȷ�Ӧ��
(3)��һ�ݻ�Ϊ2 L���ܱ������ڼ���2 mol��CO��6 mol��H2����һ�������·������·�Ӧ��CO(g)��2H2(g) ![]() CH3OH(g) ��H<0���÷�Ӧ���淴Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��
CH3OH(g) ��H<0���÷�Ӧ���淴Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��
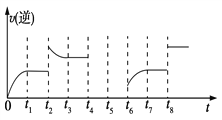
����ͼ��֪��Ӧ��t1��t3��t7ʱ���ﵽ��ƽ�⣬����t2��t8ʱ���ı������������ж�t8ʱ�ı������������________��
����t4ʱ��ѹ��t5ʱ�ﵽƽ�⣬t6ʱ����Ӧ���Ũ�ȣ�����ͼ�л���t4��t6ʱ�淴Ӧ������ʱ��Ĺ�ϵ���ߡ�________
����Ŀ����2 L�����ܱ������У�800 ��ʱ��Ӧ2NO(g)��O2(g)2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���±���
ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)ͼ�б�ʾNO2�ı仯��������________��
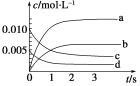
(2)��˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����________��
a��v(NO2)��2v(O2)
b��������ѹǿ���ֲ���
c��v(NO)����2v(O2)��
d�������ڵ��ܶȱ��ֲ���
(3)�ܹ�ʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����________��
a����ʱ�����NO2����
b������O2��Ũ��
����Ŀ�����в��ֶ�����Ԫ�ص����ʻ�ԭ�ӽṹ���±���
Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
T | �����������ǵ��Ӳ��������� |
X | �����������Ǵ�����������2�� |
Y | �����µ���Ϊ˫ԭ�ӷ��ӣ����⻯��ˮ��Һ�ʼ��� |
Z | Ԫ����������ǣ�7�� |
��1��Ԫ��X��һ��ͬλ�ؿɲⶨ����������ú��ص�ԭ�Ӻ�����8�����ӣ�������ͬλ�صķ�����________��
��2��Ԫ��Y�ĵ��ʵĵ���ʽΪ_________________��Ԫ��Y��Ԫ��Z���γ�һ�ָ�ԭ��������Ϊ8���ӽṹ�Ļ�����û�����ĽṹʽΪ ___________
��3��Ԫ��X��Ԫ��T��ȣ��ǽ����Խ�ǿ����Ԫ��T�����б���������֤����һ��ʵ��ѡ����_____��
a��������Ԫ��X�ĵ��ʺ�Ԫ��T�ĵ��ʵ��۷е㲻ͬ
b��Ԫ��T���⻯���Ԫ��X���⻯���ȶ�
c��Ԫ��X��Ԫ��T�ĵ��ʶ�����������ȼ��
d��Ԫ��T����������Ӧˮ��������Ա�Ԫ��X����������Ӧˮ���������ǿ
e��Na2XO3��Һ�ʼ��ԣ�Na2TO4��Һ������
��4��̽Ѱ���ʵ����ʲ�������ѧϰ����Ҫ����֮һ��T��X��Y��Z����Ԫ�ص�����������ˮ�����У���ѧ�������Բ�ͬ���������������_______________���û�ѧʽ��ʾ��
