题目内容
【题目】在2 L恒容密闭容器中,800 ℃时反应2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
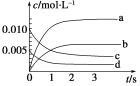
(1)图中表示NO2的变化的曲线是________。
(2)能说明该反应已经达到平衡状态的是________。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v(NO)逆=2v(O2)正
d.容器内的密度保持不变
(3)能够使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体
b.增大O2的浓度
【答案】bb、cb
【解析】
(1)根据n(NO)随时间的变化可知3 s时反应达到平衡,NO的物质的量减少0.020 mol-0.007 mol=0.013 mol,浓度减小了0.013/2=0.0065 mol·L-1,所以NO2的物质的量浓度由0增加到0.0065 mol·L-1,故b曲线正确;综上所述,本题答案是:b。
(2)a项,未指明反应进行的方向,不能判定反应是否达到平衡状态,错误;
b项,因该反应前后有气体体积的变化,即未达到平衡时,压强一直在变化,容器内压强保持不变,反应达到平衡状态,正确;
c项,用v(NO)、v(O2)表示时,方向相反,大小关系符合化学计量数之比,可以判断反应达到平衡状态,正确;
d项,根据密度ρ=m/V,因反应前后m(气)守恒,V(容)不变,故密度始终不变,无法判断反应达到平衡状态,错误;
符合题意的选项只有b、c;综上所述,本题选b、c。
(3)a项,及时分离出NO2气体,减小生成物浓度,平衡右移,反应速率减慢,不合题意,错误;
b项,增大O2的浓度,反应速率增大,平衡向正反应方向移动,符合题意,正确;
综上所述,本题选b。

【题目】向2.0 L恒容密闭容器中充入1.0 mol PCl5,在温度为T℃时发生如下反应PCl5(g) ![]() PCl3(g)+C12(g) ΔH=+124 kJ·mol-1。反应过程中测定的部分数据见下表:
PCl3(g)+C12(g) ΔH=+124 kJ·mol-1。反应过程中测定的部分数据见下表:
时间t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
回答下列问题:
(1)反应在前50 s的平均速率v(PCl5) =______________;
(2)温度为T℃时,该反应的化学平衡常数=________;
(3)要提高上述反应的转化率,可采取的措施是________ (任写一种) ;
(4)在温度为T℃时,若起始时充入0.5 mol PCl5和a mol Cl2,平衡时PCl5的转化率仍为20%,则a=________。