题目内容
【题目】室温下,向10mL pH=11的NH3·H2O溶液中加入下列物质,对所得溶液的分析正确的是( )
加入的物质 | 对所得溶液的分析 | |
A. | 90mL H2O | 由水电离出的c(H+)=10-10mol·L-1 |
B. | 0.1mol NH4Cl固体 | c(H+)比原NH3·H2O溶液中的大 |
C. | 10mL pH=13的NaOH溶液 | NH3·H2O的电离程度不变 |
D. | 10mL pH=3的盐酸 | 溶液呈中性 |
A.AB.BC.CD.D
【答案】B
【解析】
A、向10mL pH=11的NH3·H2O溶液中加入90mL H2O,由于氨水的电离,c(OH-)>10-4 mol·L-1,由水电离出的c(H+)>10-10mol·L-1,选项A错误;
B、向10mL pH=11的NH3·H2O溶液中加入0.1mol NH4Cl固体,c(NH4+)增大,电离平衡NH3·H2O![]() NH4++ OH-逆向移动,c(OH-)减小,c(H+)增大,比原NH3·H2O溶液中的大,选项B正确;
NH4++ OH-逆向移动,c(OH-)减小,c(H+)增大,比原NH3·H2O溶液中的大,选项B正确;
C、向10mL pH=11的NH3·H2O溶液中加入10mL pH=13的NaOH溶液,c(OH-)增大,抑制NH3·H2O电离,NH3·H2O的电离程度减小,选项C错误;
D、向10mL pH=11的NH3·H2O溶液中加入10mL pH=3的盐酸,NH3·H2O过量,反应后溶液呈碱性,选项D错误。
答案选B。

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案【题目】等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得到下图,则曲线a、b、c、d所对应的实验组别是
组别 | c(HCl)/molL-1 | 温度/℃ | 状态 |
1 | 2.0 | 25 | 块状 |
2 | 2.5 | 30 | 块状 |
3 | 2.5 | 50 | 粉末状 |
4 | 2.5 | 30 | 粉末状 |
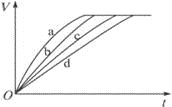
A.4-3-2-1
B.1-2-3-4
C.3-4-2-1
D.1-2-4-3