题目内容
【题目】下列事实,不能用勒夏特列原理解释的是( )
A.溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
B.对2HI(g)![]() H2(g)+I2(g),平衡体系增大压强可使颜色变深
H2(g)+I2(g),平衡体系增大压强可使颜色变深
C.反应CO+NO2![]() CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
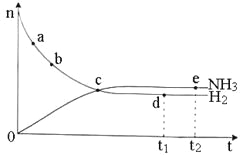
D.合成NH3反应为放热反应,为提高NH3的产率,理论上应采取低温的措施
【答案】B
【解析】
A.溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入AgNO3溶液后生成溴化银沉淀,降低溴离子浓度,平衡向正反应方向减小,溶液颜色变浅,可以用勒夏特列原理解释,A错误;
HBr+HBrO,当加入AgNO3溶液后生成溴化银沉淀,降低溴离子浓度,平衡向正反应方向减小,溶液颜色变浅,可以用勒夏特列原理解释,A错误;
B.对2HI(g)![]() H2(g)+I2(g),平衡体系增大压强,由于反应前后体积不变,平衡不移动,颜色变深是因为碘的浓度增加,与平衡移动没有关系,不能用勒夏特列原理解释,B正确;
H2(g)+I2(g),平衡体系增大压强,由于反应前后体积不变,平衡不移动,颜色变深是因为碘的浓度增加,与平衡移动没有关系,不能用勒夏特列原理解释,B正确;
C.反应CO+NO2![]() CO2+NO的正反应为放热反应,因此升高温度可使平衡向逆反应方向移动,可以用勒夏特列原理解释,C错误;
CO2+NO的正反应为放热反应,因此升高温度可使平衡向逆反应方向移动,可以用勒夏特列原理解释,C错误;
D.合成NH3反应为放热反应,为提高NH3的产率,理论上应采取低温的措施,因为低温平衡向正反应方向进行,可以用勒夏特列原理解释,D错误,
答案选B。

【题目】下列实验操作、现象与结论均正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 25℃,两片相同的Al片分别和等体积的稀HNO3和浓HNO3反应 | 前者产生无色气体,后者产生红棕色气体,且后者反应更加剧烈 | 其他条件相同时,反应物浓度越大,反应速率越快 |
B | 往黄色固体难溶物PbI2中加水,振荡,静置。取上层清液,然后加入NaI固体 | 产生黄色沉淀 | 难溶物PbI2存在沉淀溶解平衡 |
C | 向蛋白质溶液中分别加入乙醇溶液和(NH4)2SO4饱和溶液 | 均产生白色沉淀 | 蛋白质均发生了变性 |
D | 向稀硫酸中加入铜片,然后通入氧气加热 | 开始无明显现象,通入氧气加热后溶液变蓝 | 氧化性:稀硫酸> Cu2+ |
A. A B. B C. C D. D
【题目】自20世纪60年代以后,人们发现了120多种含铁硫簇![]() 如
如![]() 、
、![]() 、
、![]() 等
等![]() 的酶和蛋白质。它是存在于生物体的最古老的生命物质之一。某化学兴趣小组在研究某铁硫簇结构的组成时,设计了下列实验:
的酶和蛋白质。它是存在于生物体的最古老的生命物质之一。某化学兴趣小组在研究某铁硫簇结构的组成时,设计了下列实验:
实验一:测定硫的质量:
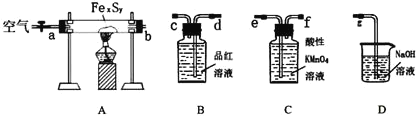
(1)连接装置,请填写接口顺序:b接____________________
(2)检查装置的气密性,在A中放入0.4g铁硫簇的样品![]() 含有不溶于水和盐酸的杂质
含有不溶于水和盐酸的杂质![]() ,在B中加入品红溶液,在C中加入30mL 0.1mol/L的酸性
,在B中加入品红溶液,在C中加入30mL 0.1mol/L的酸性![]() 溶液.
溶液.
(3)通入空气并加热,发现固体逐渐转变为红棕色.
(4)待固体完全转化后,取C中的![]() 溶液
溶液![]() ,用0.1mol/L的碘化钾
,用0.1mol/L的碘化钾![]() 溶液进行滴定。记录数据如下:
溶液进行滴定。记录数据如下:
滴定次数 | 待测溶液体积 | 消耗碘化钾溶液体积 | |
滴定前刻度 | 滴定后刻度 | ||
1 |
|
|
|
2 |
|
|
|
3 |
|
|
|
实验二:测定铁的质量:
取实验Ⅰ中A的硬质玻璃管中的残留固体加入稀盐酸中,充分搅拌后过滤,在滤液中加入足量的NaOH溶液,过滤后取滤渣,经灼烧得0.32g固体.试回答下列问题:
(1)检查“实验一”中装置A的气密性的方法是_________
(2)滴定终点的判断方法是_________
(3)装置B中品红溶液的作用是_______![]() 有同学提出,撤去B装置,对实验没有影响,你的看法是______
有同学提出,撤去B装置,对实验没有影响,你的看法是______![]() 选填“合理”或“不合理”
选填“合理”或“不合理”![]() ,理由是_________
,理由是_________
(4)用KI溶液滴定![]() 溶液时发生反应的离子方程式为_________
溶液时发生反应的离子方程式为_________
(5)请计算这种铁硫簇结构的化学式_________
(6)下列操作,可能引起![]() 偏大的是_________
偏大的是_________
![]() 滴定剩余
滴定剩余![]() 溶液时,KI溶液滴到锥形瓶外边一滴
溶液时,KI溶液滴到锥形瓶外边一滴
![]() 配制KI溶液时,定容时俯视刻度线
配制KI溶液时,定容时俯视刻度线
![]() 用碘化钾溶液滴定剩余
用碘化钾溶液滴定剩余![]() 溶液时,滴定前有气泡,滴定后无气泡
溶液时,滴定前有气泡,滴定后无气泡
![]() 实验二中,对滤渣灼烧不充分
实验二中,对滤渣灼烧不充分